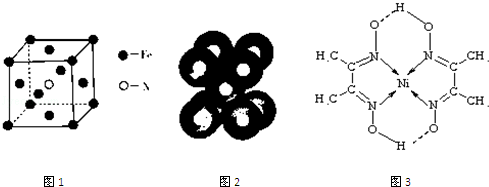
4.莫尔盐[(NH4)2Fe(SO4)2•6H2O]常作氧化还原滴定法的基准物质,下列有关该盐溶液的比较,不正确的是( )
| A. | c(SO42-)>c(NH4+)>c(Fe2+)>c(H+)>c(OH-) | B. | c(SO42-)=c(NH4+)>c(Fe2+)>c(H+)>c(OH-) | ||
| C. | 2c(SO42-)+c(OH-)=c(NH4+)+2c(Fe2+)+c(H+) | D. | c(NH4+)+c(NH3•H2O)=2c(Fe2+)+2c[Fe(OH)2] |
1.根据表中信息判断,下列选项正确的是( )
| 序号 | 反应物 | 产物 |
| 1 | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4… |
| 2 | Cl2、FeBr2 | FeCl3、FeBr3 |
| 3 | MnO4-、Cl-… | Cl2、Mn2+… |
| A. | 第①组反应的其余产物为H20 | |
| B. | 第②组反应中CI2与FeBr2的物质的量之比小于或等于1:2 | |
| C. | 第③组反应中生成1mol Cl2,转移电子5 mol | |
| D. | 氧化性由强到弱顺序为Mn04->Cl2>Fe3+>Br2 |
20.已知硫酸亚铁溶液中加入过氧化钠时发生反应:4Fe2++4Na2O2+6H2O=4Fe(OH)3↓+O2↑+8Na+,则下列说法不正确的是( )
| A. | 反应过程中可以看到白色沉淀先转化为灰绿色后转化为红褐色 | |
| B. | 若Fe2+失去4mol电子,生成氧气的体积在标准状况下约为22.4L | |
| C. | 4 mol Na2O2在反应中共得到6NA个电子 | |
| D. | 该反应中Na2O2既是氧化剂又是还原剂,O2是氧化产物 |
19.茶叶中铁元素的检验可经过以下四个步骤完成,各步骤中选用的实验用品不能都用到的是( )(Fe3+的检验滴加KSCN溶液)
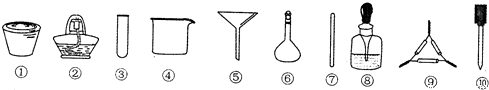

| A. | 将茶叶灼烧灰化,选用①、②和⑨ | |
| B. | 检验滤液中的Fe3+,选用③、⑧和⑩ | |
| C. | 用浓硝酸溶解茶叶灰并加蒸馏水稀释,选用④、⑥和⑦ | |
| D. | 过滤得到的滤液,选用④、⑤和⑦ |
15.工业上用某矿渣(主要成分是Cu2O,少量杂质是Al2O3、Fe2O3和SiO2)提取铜的操作流程如下:
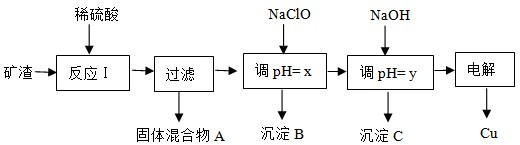
已知:Cu2O+2H+=Cu+Cu2++H2O
(1)固体混合物A中的成分是SiO2、Cu(填化学式).
(2)反应I完成后,铁元素的存在形式为Fe2+(填离子符号).
(3)y的数值范围是5.2≤pH<5.4.
(4)若电解法获得Cu 64.0g,则原矿渣中Cu2O的质量是c.
a、144.0gb、大于144.0g c、小于144.0g
(5)下列关于用NaClO调节溶液pH的说法正确的是b.
a、加入NaClO可使溶液的pH降低
b、NaClO能调节pH的主要原因是由于发生反应:ClO-+H+=HClO,ClO-消耗H+,从而达到调节pH的目的
c、NaClO能调节pH的主要原因是由于NaClO水解:ClO-+H2O?HClO+OH-消耗H+,从而达到调节pH的目的.
(6)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,且该物质与还原产物的物质的量之比为4:1,该反应的离子方程式为2Fe2++5ClO-+5H2O=2Fe(OH)3+Cl-+4HClO.
0 151805 151813 151819 151823 151829 151831 151835 151841 151843 151849 151855 151859 151861 151865 151871 151873 151879 151883 151885 151889 151891 151895 151897 151899 151900 151901 151903 151904 151905 151907 151909 151913 151915 151919 151921 151925 151931 151933 151939 151943 151945 151949 151955 151961 151963 151969 151973 151975 151981 151985 151991 151999 203614

已知:Cu2O+2H+=Cu+Cu2++H2O
| 沉淀 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 5.4 | 4.0 | 2.2 | 5.8 |
| 沉淀完成pH | 6.7 | 5.2 | 3.2 | 8.8 |
(2)反应I完成后,铁元素的存在形式为Fe2+(填离子符号).
(3)y的数值范围是5.2≤pH<5.4.
(4)若电解法获得Cu 64.0g,则原矿渣中Cu2O的质量是c.
a、144.0gb、大于144.0g c、小于144.0g
(5)下列关于用NaClO调节溶液pH的说法正确的是b.
a、加入NaClO可使溶液的pH降低
b、NaClO能调节pH的主要原因是由于发生反应:ClO-+H+=HClO,ClO-消耗H+,从而达到调节pH的目的
c、NaClO能调节pH的主要原因是由于NaClO水解:ClO-+H2O?HClO+OH-消耗H+,从而达到调节pH的目的.
(6)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,且该物质与还原产物的物质的量之比为4:1,该反应的离子方程式为2Fe2++5ClO-+5H2O=2Fe(OH)3+Cl-+4HClO.