3.室温下,某氨水pH=x,某盐酸pH=y,已知x+y=14,且x>11.将上述氨水、盐酸等体积混合后,所得溶液中各种离子浓度由大到小的顺序正确是( )
| A. | c(NH4+)>c(Cl-)>c(OH-)>c(H+) | B. | c(Cl-)>c(NH4+)>c(H+)>c(OH-) | ||
| C. | c(Cl-)=c(NH4+)>c(OH-)=c(H+) | D. | c(Cl-)=c(NH4+)>c(OH-)>c(H+) |
2.常温下,在BaSO4饱和溶液中加入Na2SO4固体,达到溶解平衡时,下列说法正确的是( )
| A. | c(Ba2+)=c(SO42-) | |
| B. | c(Ba2+)增大,c (SO42-) 减小 | |
| C. | c(Ba2+)≠c SO42-),c(Ba2+)•c(SO42-)=KSP(BaSO4) | |
| D. | c(Ba2+)≠c(SO42-),c(Ba2+)•c(SO42-)≠KSP(BaSO4) |
1.用NA表示阿伏加德罗常数,下列说法中正确的是( )
| A. | 23g Na完全转化生成Na2O和Na2O2,失去电子数为NA 到2NA之间 | |
| B. | 常温常压下,46g由NO2和N2O4组成的混合气体中含有原子的总数为3NA | |
| C. | 含2mol H2SO4的浓硫酸与足量铜微热反应,生成SO2分子数为NA | |
| D. | 粗铜精炼时转移1mol电子,阳极上溶解的Cu原子数一定为0.5 NA |
20.用下列装置能达到有关实验目的是( )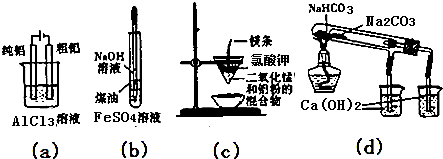

| A. | 用图(a)装置电解精炼铝 | |
| B. | 用图(b)装置制备Fe(OH)2 | |
| C. | 图(c)装置可制得金属钾 | |
| D. | 图(d)验证NaHCO3和Na2CO3的热稳定性 |
18.下列各醇,能发生催化氧化的是( )
| A. | 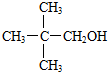 | B. |  | C. | 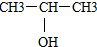 | D. | 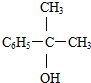 |
17.我国晋朝傅玄的《傅鹑觚集•太子少傅箴》中写道:“夫金木无常,方园应行,亦有隐括,习与性
形.故近朱者赤,近墨者黑.”这里的“朱”指的是( )
形.故近朱者赤,近墨者黑.”这里的“朱”指的是( )
| A. | Fe3 04 | B. | CuO | C. | HgS | D. | FeS |
16.设阿伏加德罗常数的数值为NA,下列说法不正确的是( )
| A. | 46 g的NO2和N2O4混合气体含有的原子数为3NA | |
| B. | 1 mol Na2O2与足量H2O反应,转移的电子数为NA | |
| C. | 物质的量浓度为0.5 mol/L MgCl2溶液,含有Cl-离子数为NA | |
| D. | 2.7g铝与足量的盐酸或氢氧化钠溶液反应,生成H2的分子数均为0.15NA |
15.关于如图各实验装置的叙述中,不正确的是( )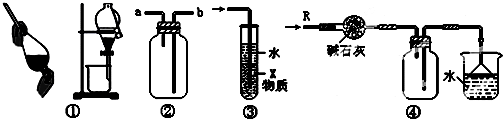
0 151803 151811 151817 151821 151827 151829 151833 151839 151841 151847 151853 151857 151859 151863 151869 151871 151877 151881 151883 151887 151889 151893 151895 151897 151898 151899 151901 151902 151903 151905 151907 151911 151913 151917 151919 151923 151929 151931 151937 151941 151943 151947 151953 151959 151961 151967 151971 151973 151979 151983 151989 151997 203614

| A. | 装置①可用于分离乙醇和水的混合物 | |
| B. | 装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体 | |
| C. | 装置③中X若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸 | |
| D. | 装置④可用于干燥、收集氨气,并吸收多余的氨气 |