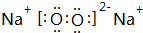
14.下列说法不正确的是( )
| A. | 将wg质量分数为 a%的NaCl溶液加入wg水,得到的NaCl溶液质量分数一定为a/2% | |
| B. | 将wg质量分数为 a%的NaCl溶液蒸发掉w/2g水,得到的NaCl溶液质量分数一定为2a% | |
| C. | 现有10%和30%的氨水等质量混合后,溶液里溶质的质量分数为20% | |
| D. | 室温下向100ml1.2mol/l饱和石灰水中加入1.5g生石灰后恢复室温,石灰水中Ca(OH)2的物质的量不变 |
12.已知25%酒精的密度为0.91g•cm-3,5%的酒精密度为0.98g•cm-3,如果将上述两种溶液等体积混合,所得酒精的质量分数( )
| A. | 等于15% | B. | 大于15% | C. | 小于15% | D. | 无法估算 |
11.下列陈述 I、II正确并且有因果关系的是( )
| 选项 | 叙述I | 叙述II |
| A | 锌金属活动性比铁强 | 海轮外壳上装锌块可减缓腐蚀 |
| B | Ba(OH)2可与盐酸反应 | Ba(OH)2可用于治疗胃酸过多 |
| C | SiO2是酸性氧化物 | SiO2能与水反应生成硅酸 |
| D | H2O2有氧化性 | H2O2能使酸性高锰酸钾溶液褪色 |
| A. | A | B. | B | C. | C | D. | D |
10.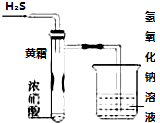 某同学用下列实验装置探究硝酸的性质.根据图示判断下列结论不正确的是
某同学用下列实验装置探究硝酸的性质.根据图示判断下列结论不正确的是
( )
 某同学用下列实验装置探究硝酸的性质.根据图示判断下列结论不正确的是
某同学用下列实验装置探究硝酸的性质.根据图示判断下列结论不正确的是( )
| A. | 试管内壁上“黄霜”的成分是硫 | |
| B. | 该实验探究说明浓硝酸既有氧化性,又有挥发性 | |
| C. | 烧杯内的NaOH溶液的作用是除去尾气,防止尾气污染环境 | |
| D. | H2S用SO2代替,将无明显反应现象 |
9.氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于阴影部分的是( )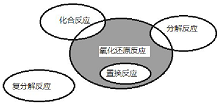

| A. | Cl2+2KBr═Br2+2Cl2 | B. | 2Na2O2+2CO2═2Na2CO3+O2 | ||
| C. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 | D. | 2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$ Na2CO3+H2O+CO2↑ |
7.茫茫黑夜中,航标灯为航海员指明了方向.航标灯的电源必须长效、稳定.我国科技工作者研制出以铝合金、Pt-Fe合金网为电极材料的海水电池.在这种电池中①铝合金是阳极 ②铝合金是负极 ③海水是电解液 ④铝合金电极发生还原反应( )
| A. | ②③ | B. | ②④ | C. | ①② | D. | ①④ |
6.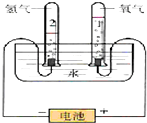 水是人类宝贵的自然资源,也是一种重要的化工原料.如图是电解水原理的实验装置图.
水是人类宝贵的自然资源,也是一种重要的化工原料.如图是电解水原理的实验装置图.
(1)写出电解水的化学方程式,若为氧化还原反应,请用双线桥表示出电子的转移方向和数目.
 .
.
(2)假设电解了3.6gH2O,请完成下表.
(3)若在47.8gH2O(过量)中加入2.3gNa.钠与水反应的离子方程式为2Na+2 H2O═2Na++2OH-+H2↑,,反应后得到的溶液中溶质是NaOH,溶质的质量分数为8%,若要计算该溶液中溶质的物质的量浓度,则还需要溶液密度(填物理量).
(4)若在电解水后收集到O2体积为22.4mL(在标准状况下),则收集到的H2的质量0.004g.
 水是人类宝贵的自然资源,也是一种重要的化工原料.如图是电解水原理的实验装置图.
水是人类宝贵的自然资源,也是一种重要的化工原料.如图是电解水原理的实验装置图.(1)写出电解水的化学方程式,若为氧化还原反应,请用双线桥表示出电子的转移方向和数目.
 .
.(2)假设电解了3.6gH2O,请完成下表.
| 质 量 | 物质的量 | O2与H2的体积比(同温同压下) | |
| O2 | 3.2g | 0.1mol | 1:2 |
| H2 | 0.4g | 0.2mol |
(4)若在电解水后收集到O2体积为22.4mL(在标准状况下),则收集到的H2的质量0.004g.
5.下列关于金属腐蚀的说法正确的是( )
0 151796 151804 151810 151814 151820 151822 151826 151832 151834 151840 151846 151850 151852 151856 151862 151864 151870 151874 151876 151880 151882 151886 151888 151890 151891 151892 151894 151895 151896 151898 151900 151904 151906 151910 151912 151916 151922 151924 151930 151934 151936 151940 151946 151952 151954 151960 151964 151966 151972 151976 151982 151990 203614
| A. | 金属在潮湿的空气中腐蚀的实质是:M+nH2O═M(OH)n+$\frac{n}{2}$H2↑ | |
| B. | 金属的化学腐蚀的实质是:M-ne-═Mn+,电子直接转移给还原剂 | |
| C. | 金属的化学腐蚀必须在酸性条件下进行 | |
| D. | 在潮湿的中性环境中金属的电化学腐蚀主要是吸氧腐蚀 |