通过实验、观察、类比、推理等方法得出正确的结论是化学学习的方法之一.对下列反应的推断或解释正确的是( )
选项 | 操作 | 可能的实验现象 | 解释 |
A | 某溶液中加入硝酸酸化的氯化钡溶液 | 有白色沉淀生成 | 溶液中一定含有SO42﹣ |
B | 向淀粉KI溶液中不断通入C12 | 溶液变蓝后褪色 | C12先表现氧化性后表现漂白性 |
C | CO还原Fe2O3得到的黑色固体加入盐酸溶解后再加入KSCN溶液 | 溶液不显红色 | 黑色固体没有Fe3O4 |
D | 将SO2通入BaCl2溶液中 | 没有白色沉淀生成 | BaSO3可溶于酸 |
为处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏.化学家研究在催化条件下,通过反应CCl4+H2 CHCl3+HCl△H<O,使CCl4转化为重要的化工原料氯仿(CHCl3).已知CCl4的沸点为77℃,CHCl3的沸点为61.2℃.在密闭容器中,该反应达到平衡后,测得如下数据.
CHCl3+HCl△H<O,使CCl4转化为重要的化工原料氯仿(CHCl3).已知CCl4的沸点为77℃,CHCl3的沸点为61.2℃.在密闭容器中,该反应达到平衡后,测得如下数据.
实验序号 | 温度℃ | 初始CCl4浓度(mol·L﹣1) | 初始H2浓度(mol·L﹣1) | CCl4的转化率 |
1 | 110 | 1 | 1 | 50% |
2 | 100 | 1 | 1 | x |
3 | 110 | 0.8 | y | 60% |
(1)实验1中,10h后反应达到平衡,则从反应开始至达到平衡状态,H2的平均反应速率为 mol·L﹣1·h﹣1.在此实验的平衡体系中,再加入0.5mol CCl4和0.5mol HCl,平衡将怎样移动? (填“向左移动”、“向右移动”、“不移动”或“无法确定”).
(2)实验2中,x为 (填字母).
A.等于50% B.大于50% C.小于50% D.无法确定
(3)实验3中的y为 .
(4)在100℃条件下,能说明反应CCl4+H2 CHCl3+HCl△H<O达到平衡状态的是 (填字母).
CHCl3+HCl△H<O达到平衡状态的是 (填字母).
A.压强不再变化 B.生成HCl的速率和消耗H2的速率相等
C.混合气体的密度不变 D.H2的质量不再变化
(5)用电解法处理高浓度重铬酸钠废水具有效果稳定可靠,操作管理简单,设备占地面积小,废水中的重金属离子也能通过电解有所降低等优点,其原理是铁作电极,在酸性条件下,将Cr6+还原为Cr3+,其装置示意图如图所示.
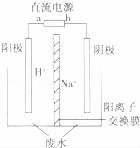
若以甲醚燃料电池为直流电源(电解质溶液为KOH溶液),则燃料电池中b极应通入 ,a极的电极反应为 .
能否用铜作电解重铬酸钠废水的电极? (填“能”或“不能”),理由是
③除去重铬酸根离子的离子反应是 .
 。合成路线如下:
。合成路线如下:


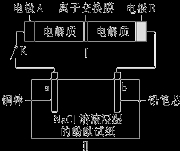
 2Na2S2+NaBr3.闭合开关K时,b极附近先变红色.下列说法正确的是( )
2Na2S2+NaBr3.闭合开关K时,b极附近先变红色.下列说法正确的是( )