短周期元素X、Y、Z、W、Q在元素周期表中的位置如表所示,其中W的气态氢化物摩尔质量为34 g/mol,则下列说法中不正确的是
| X | Y |
|
Z |
| W | Q |
A.阴离子还原性:W>Q
B.X的最低价氢化物能形成分子间氢键
C.Z能在自然界中以游离态存在
D.Na与Y能形成化合物Na2Y2,1 mol Na2Y2与CO2反应,转移电子数为1 NA
已知有反应:2A(g)+B(g) 3C(g);△H<0,在恒容的密闭容器中,通入A和B气体,反应达到平衡后,若仅改变图中x的值,则y随x变化趋势合理的是
3C(g);△H<0,在恒容的密闭容器中,通入A和B气体,反应达到平衡后,若仅改变图中x的值,则y随x变化趋势合理的是
选项 | X | Y |
|
A | 温度 | 容器内混合气体的密度 | |
B | A的物质的量 | B的转化率 | |
C | 催化剂的质量 | C的体积分数 | |
D | 加入Ar的物质的量 | 逆反应速率 |
X、Y、Z、P、Q、W、R、T是元素周期表短周期中的常见主族元素,且原子序数依次增大,其相关信息如下表:
元素 | 相关信息 |
X | 其一种同位素,可被用作相对原子质量的标准 |
Y | 其最高价氧化物对应水化物能与其气态氢化物相互间发生化合反应 |
P | 是短周期中(除稀有气体外)原子半径最大的元素 |
Q | 存在质量数为25,中子数为13的核素 |
W | 位于周期表第13列 |
R | 与Z同族,且最高价氧化物对应水化物的浓溶液常温下与W单质会出现钝化现象 |
(1)R在元素周期表中的位置为 ;将Q、W、Z、Y的简单离子的半径从大到小排序___________________________________________(用离子符号表示)
(2)T的单质易溶于XT4中,理由是:____________________________________________。
(3)根据下表中信息,判断下列化合物固态的晶体类型(填“离子晶体”… 等):
化合物 | X3Y4 | R2T2 |
晶体类型 |
|
|
熔点/℃ | >3600 | -76 |
(4)任意写出一个由Y、Z元素分别与氢元素形成的10电子粒子间相互反应的离子方程式:___________。
(5)在25℃、101 kPa下,已知13.5 g的W固体单质在Z2气体中完全燃烧后恢复至原状态,放热419 kJ,写出表示W单质燃烧热的热化学方程式 。
(6)化合物P2R溶液在空气中长期放置,与氧气反应会生成与过氧化钠的结构相似的物质P2R2,其溶液显黄色,则P2R2的电子式为 ,用化学方程式表示P2R溶液在空气中的变质过程 。
 2HI(g);△H= -9.48kJ/mol
2HI(g);△H= -9.48kJ/mol  C.反应(i)的产物比反应(ii)的产物稳定
C.反应(i)的产物比反应(ii)的产物稳定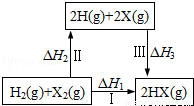
 2SO3(g);△H<0,在一恒容容器中,由SO2和O2开始反应,下列说法正确的是
2SO3(g);△H<0,在一恒容容器中,由SO2和O2开始反应,下列说法正确的是  2NH3,下列说法错误的是
2NH3,下列说法错误的是 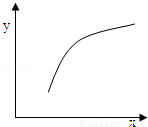
 xQ(g)+ 3R(g),该反应达到平衡时生成2.4 mol R,并测得Q浓度为0.4 mol/L,下列叙述正确的是
xQ(g)+ 3R(g),该反应达到平衡时生成2.4 mol R,并测得Q浓度为0.4 mol/L,下列叙述正确的是