(NH4)2Fe(SO4)2•6H2O(莫尔盐,浅绿色,式量392)在定量分析中常用作标定高锰酸钾、重铬酸钾等溶液的标准物质,还用作化学试剂、医药以及用于冶金、电镀等。
回答下列问题:
(1)莫尔盐在空气中比硫酸亚铁稳定,但长期露置于空气中也会变质,检验莫尔盐是否变质的试剂是________;
(2)准确称取mg纯净的莫尔盐,在锥形瓶中加人20mL水充分溶解,用某酸性K2Cr2O7溶液滴定至终点.重复进行3次,测得有关数据如下:
实验序号 | 起始读数/mL | 终点读数/mL |
I | 2.50 | 22.58 |
Ⅱ | 1.00 | 23.12 |
Ⅲ | 0.00 | 19.92 |
①K2Cr2O7溶液应该放在________式滴定管中.
②写出滴定过程中反应的离子方程式:________;
③所测K2Cr2O7溶液的物质的量浓度为________mol/L(用含M的代数式表示)
(3)某课题组通过实验检验莫尔盐晶体加热时的分解产物。
①甲同学提出猜想:分解产物可能是N2、Fe2O3,SO3、H2O四种物质.你是否同意并说明理由:________;
②乙同学设计了如图装置,其中A装置中的固体变为红棕色,则固体产物中含有________;C装置中红色褪去,说明气体产物中含有________;C装置后应连接尾气吸收装置D,D中盛有的试剂可以是________(写一种即可)。
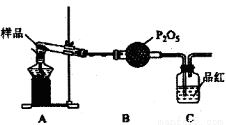
③丙同学想利用上述装置证明分解产物中含有氨气.只需更换B,C中的试剂即可,则更换后的试剂为B________、C________;
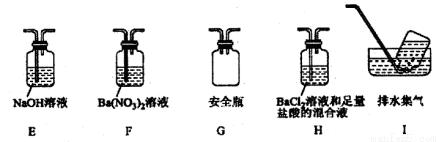
④丁同学认为莫尔盐分解可能会生成N2,SO3,拟从下列装置如图2中选择必要的装置加以证明.则正确的连接顺序从左到右依次是A、________。
卤族元素的单质和化合物很多我们可以利用所学物质结构与性质的相关知识去认识和理解它们。
(1)卤族元素位于周期表的________区;溴的价电子排布式为________;
(2)请根据如表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是________。
| 氟 | 氯 | 溴 | 碘 | 铍 |
第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 | 900 |
(3)已知高碘酸有两种形式,化学式分别为H5IO6(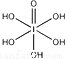 )和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6________ HIO4.(填“>”、“<”或“=”)
)和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6________ HIO4.(填“>”、“<”或“=”)
(4) 与KI3类似的,还有CsICl2等.已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列________式发生.
A.CsICl2=CsCl+ICl B.CsICl2=CsI+Cl2
(5)已知ClO2-为角型,氯原子的杂化轨道类型为________,与ClO2-互为等电子体的微粒是________。(任写一个)
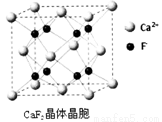
(6)下图为碘晶体晶胞结构.有关说法中正确的是________
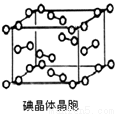
A.碘分子的排列有2种不同的取向,2种取向不同的碘分子以4配位数交替配位形成层结构
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中存在的相互作用有非极性键和范德华力
(7)已知CaF2晶体(见图)的密度为ρg/cm3,NA为阿伏加德罗常数,相邻的两个Ca2+的核间距为a cm,则CaF2的相对分子质量可以表示为________。

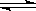 AgI(s)+Br-(aq) 的平衡常数K=200
AgI(s)+Br-(aq) 的平衡常数K=200 N2(g)+2CO2(g)△H=akJ/mol
N2(g)+2CO2(g)△H=akJ/mol 

 = ________己知该温度下,NH3·H2O的Kb=1.7×10-5)
= ________己知该温度下,NH3·H2O的Kb=1.7×10-5) 的值将________(填“变大”、“不变”或“变小”)
的值将________(填“变大”、“不变”或“变小”)
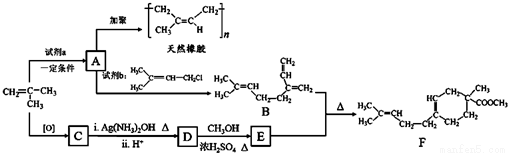
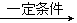
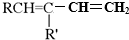
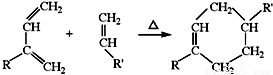 (R、R′可以是氢原子、烃基或官能团)
(R、R′可以是氢原子、烃基或官能团)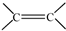 和
和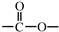 结构的D的所有同分异构共有________种(不包括顺反异构体),写出其中任意两种的结构简式________。
结构的D的所有同分异构共有________种(不包括顺反异构体),写出其中任意两种的结构简式________。
 2Z(g)一定达到化学平衡状态的是( )
2Z(g)一定达到化学平衡状态的是( ) H2CO3+2OH-
H2CO3+2OH-