0 149370 149378 149384 149388 149394 149396 149400 149406 149408 149414 149420 149424 149426 149430 149436 149438 149444 149448 149450 149454 149456 149460 149462 149464 149465 149466 149468 149469 149470 149472 149474 149478 149480 149484 149486 149490 149496 149498 149504 149508 149510 149514 149520 149526 149528 149534 149538 149540 149546 149550 149556 149564 203614
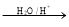 R-CH2CHO + R′OH(烃基烯基醚)烃基烯基醚A的相对分子质量(Mr)为176,分子中碳氢原子数目比为3∶4 。与A相关的反应如下:
R-CH2CHO + R′OH(烃基烯基醚)烃基烯基醚A的相对分子质量(Mr)为176,分子中碳氢原子数目比为3∶4 。与A相关的反应如下: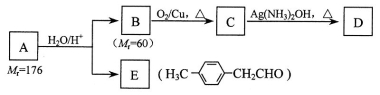
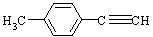 )的一条路线如下:
)的一条路线如下:
 乙、丙、X是中学化学中常见的4种物质,其转化关系符合下图。其中甲和X可能是( )
乙、丙、X是中学化学中常见的4种物质,其转化关系符合下图。其中甲和X可能是( )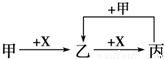

 氯水,反应中有0.3NA电子转移
氯水,反应中有0.3NA电子转移
 .若HnAOm是强酸,则A元素的氢化物的水溶液一定显酸性
.若HnAOm是强酸,则A元素的氢化物的水溶液一定显酸性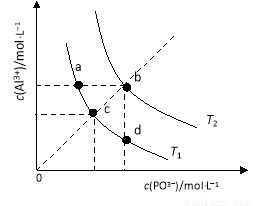
 d
d Al3+(aq)+PO43?(aq) △H<0
Al3+(aq)+PO43?(aq) △H<0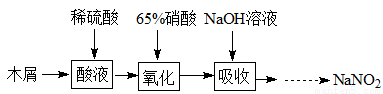
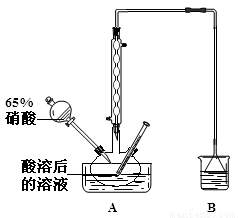
 积为V mL。
积为V mL。