0 149046 149054 149060 149064 149070 149072 149076 149082 149084 149090 149096 149100 149102 149106 149112 149114 149120 149124 149126 149130 149132 149136 149138 149140 149141 149142 149144 149145 149146 149148 149150 149154 149156 149160 149162 149166 149172 149174 149180 149184 149186 149190 149196 149202 149204 149210 149214 149216 149222 149226 149232 149240 203614


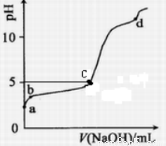
 Al(OH)3
Al(OH)3