如图装置可用于收集气体并验证其某些化学性质,你认为正确的是
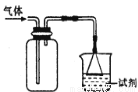
选项 | 气体 | 试剂 | 现象 | 结论 |
A | NH3 | 酚酞试液 | 溶液变红色 | NH3的水溶液显碱性 |
B | Cl2 | 紫色石蕊试液 | 溶液先变红后褪色 | Cl2有酸性和漂白性 |
C | C2H2 | 溴水 | 溶液褪色 | C2H2分子中含碳碳双键 |
D | X | Kl淀粉溶液 | 溶液变蓝 | X 可能是Cl2或NO2 |
(15分)硅孔雀石的主要成分为CuCO3•Cu(OH)2和CuSiO3•2H2O,还含有SiO2、FeCO3、Fe2O3、Al2O3等杂质。以硅孔雀石为原料制取硫酸铜的工艺流程如下:
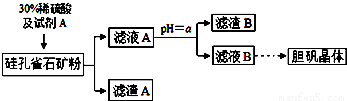
部分氢氧化物开始沉淀和完全沉淀的pH如下表
氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 |
完全沉淀的pH | 5.2 | 3.7 | 9.7 | 6.7 |
请回答下列问题:
(1)滤渣B的主要成分是 (用化学式表示);判断本实验能否调节溶液pH使杂质完全除去而不损失Cu2+,并简述理由 。
(2)用离子方程式表示加入绿色氧化剂A的作用 。
(3)可向滤液A中加入 (填字母)调节PH以除去杂质
a.氨水 b.氧化铜 c.氢氧化钠 d.氢氧化铜
(4)从滤液B中提取胆矾的操作包括 、用乙醇洗涤、用滤纸吸干等。
(5)测定产品纯度和胆矾中结晶水数目
①沉淀法测定产品纯度
取一定质量的样品溶于蒸馏水,加入足量的BaCl2溶液和稀硝酸,过滤、洗涤、干燥、称重,实验结果发现测得的产品纯度偏高,可能的原因是 填字母)
a.产品失去部分结晶水 b.产品中混有CuCl2•2H2O
c.产品中混有Al2(SO4)3•12H2O d.产品中混有Na2SO4
②差量法测得结晶水数目
取ag样品盛装在干燥的坩锅里,灼烧至结晶水全部失去,称得无水硫酸铜的质量b g,则胆矾(CuSO4•nH2O)中n值的表达式为 。
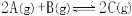 , 若经2s后测得C的浓度为0.6mol.L-1,下列几种说法,其中正确的是
, 若经2s后测得C的浓度为0.6mol.L-1,下列几种说法,其中正确的是