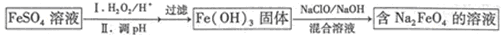(9分)下表是甲、乙、丙、丁四种有机物的有关信息;
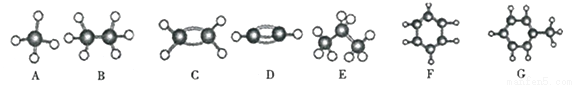
甲 | ①能使溴的四氯化碳溶液褪色;②比例模型为: |
乙 | ①由C、H两种元素组成;②球棍模型为 |
丙 | ①由C、H、O三种元素组成;②能与Na反应,但不能与NaOH溶液反应;③能与丁反应生成戊 |
丁 | ①由C、H、O三种元素组成;②球棍模型为 |
根据表中信息回答下列问题:
(1)写出与甲互为同系物,且比甲多一个碳原子的有机物在一定条件下生成的高分子化合物的结构简式 ;
(2)乙与液溴反应的化学方程式为 ;
(3)丙与丁反应能生成戊,戊为相对分子质量为100的酯,该反应类型为 ,其化学反应方程式为 ;(4)写出一种符合下列条件的戊的同分异构体的结构简式: ;
I.分子中不含支链并能使溴的四氯化碳溶液褪色
II.能与NaHCO3溶液发生反应
煤化工中两个重要反应为①C(s)+H2O(g)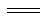 H2(g)+CO(g)ΔH=+131.3 kJ·mol-1,②CO(g)+ H2O(g)
H2(g)+CO(g)ΔH=+131.3 kJ·mol-1,②CO(g)+ H2O(g) CO2(g)+ H2(g)。
CO2(g)+ H2(g)。
(1)下列说法正确的是 。
A.当反应①的容器中混合气体的密度不再变化时反应达到最大限度
B.反应②的熵变△S>0
C.反应①中增加C固体的量能增大反应速率
D.在反应中②及时分离出产生的H2对正反应速率无影响
(2)若工业上要增加反应①的速率,最经济的措施为 。
(3)现将不同量的CO(g)和H2O(g)分别通入2L恒容密闭容器中进行反应,得到如下三组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/ min | ||
CO | H2O | H2 | CO2 | |||
I | 650 | 4 | 2 | 1.6 | 1.6 | 5 |
Ⅱ | 900 | 2 | 1 | 0.5 | 0.5 | 3 |
Ⅲ | 900 | a | b | c | d | t |
①实验I中,从反应开始到反应达到平衡时,H2O的平均反应速率为___。
②CO(g)和H2O(g)反应的△H 0(填“大于”、“小于”或“等于”)
③实验III中,若平衡时,CO的转化率大于水蒸气,则a、b必须满足的关系是______,与实验Ⅱ相比,化学平衡常数 (填“增大”、“减小”或“不变”)。
④若在900℃时,实验II反应达到平衡后,向此容器中再加入1 mol CO、0.5 mol H2O、0.2 mol CO2、0.5 mol H2,平衡向__________方向移动(填“正反应”、“逆反应”“不移动”)。
(4)CO、H2可用于甲醇和甲醚,其反应为(m、n均大于0):
反应①:CO(g)+2H2(g) CH3OH(g)ΔH= -mkJ·mol-1
CH3OH(g)ΔH= -mkJ·mol-1
反应②: 2CO(g)+4 H2(g) CH3OCH3(g)+H2O(g)ΔH=-nkJ·mol-1
CH3OCH3(g)+H2O(g)ΔH=-nkJ·mol-1
反应③:2CH3OH(g) CH3OCH3(g)+ H2O(g)△H<0
CH3OCH3(g)+ H2O(g)△H<0
则m与n的关系为 。
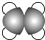 ③能与水在一定条件下反应生成丙
③能与水在一定条件下反应生成丙