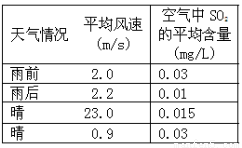
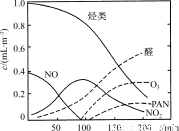
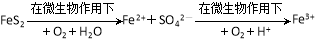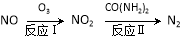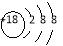下列陈述Ⅰ、Ⅱ正确并有因果关系的是
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | 氢氟酸具有酸性 | 氢氟酸可用于雕刻玻璃 |
B | 氯水显酸性 | 可用pH试纸测氯水的pH |
C | NH3极易溶于水 | NH3可用作制冷剂 |
D | ClO2具有强氧化性 | ClO2可用于自来水的杀菌消毒 |
【离子推断】(15分)某混合溶液中,只可能大量含有下表所列离子中的某几种:
阳离子 | H+、K+、Al3+、NH4+、Mg2+ |
阴离子 | OH-、SO42-、CO32-、AlO2-、S2- |
将Na2O2逐渐加入到上述混合溶液中,产生沉淀的物质的量与加入Na2O2的物质的量的关系如图所示。

(1)将上述混合溶液中一定大量含有的阴、阳离子及其物质的量填入下表(可以不填满,也可以增加)。(每空1分)
离子种类 | ||||||
物质的量(mol) |
(2)图中a=____________,(2分) b=____________。(3分)