下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
物质 编号 | 物质转化关系 | 甲 | 乙 | 丙 | 丁 |
① |
| Cu | CuO | CuSO4 | Cu(NO3)2 |
② | Na2CO3 | NaOH | NaHCO3 | CO2 | |
③ | (NH4)2SO3 | CaSO3 | SO2 | NH4HSO3 | |
④ | Fe | FeCl3 | FeCl2 | Fe(NO3)2 |
A.①②③④ B.①②③ C.①③④ D.②④
下列实验的现象与对应结论均正确的是
选项 | 操作 | 现象 | 结论 |
A | 将铁片插入到硫酸铜溶液中 | 铁片表面呈紫红色 | 铁单质的氧化性强于铜单质 |
B | 常温下将Al片放入浓硝酸中 | 无明显变化 | Al与浓硝酸不反应 |
C | 将一小块Na放入无水乙醇中 | 产生气泡 | Na能置换出醇羟基中的氢 |
D | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下发生反应 |
 2NH3(g)ΔH=-92 kJ/mol放出热量9.2kJ时,转移电子0.6NA
2NH3(g)ΔH=-92 kJ/mol放出热量9.2kJ时,转移电子0.6NA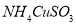 与足量的10mol/L硫酸液混合微热,产生下列现象:①有红色金属生成 ②产生刺激性气味的气体 ③溶液呈现蓝色。据此判断下列说法正确的是
与足量的10mol/L硫酸液混合微热,产生下列现象:①有红色金属生成 ②产生刺激性气味的气体 ③溶液呈现蓝色。据此判断下列说法正确的是 中硫元素被氧化
中硫元素被氧化 完全反应转移0.5mol电子
完全反应转移0.5mol电子
