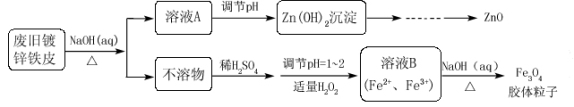
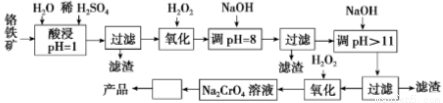
Ⅰ以铬铁矿(主要成分是FeO·Cr2O3,含少量MgCO3、Al2O3、SiO2等)为原料制取Na2CrO4晶体的工艺流程如下:
已知:①+3价Cr在酸性溶液中性质稳定,当pH>9时以CrO 形式存在且易氧化;②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
形式存在且易氧化;②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
开始沉淀时的pH | 2.7 | 7.6 | 9.0 | —— | —— |
沉淀完全时的pH | 3.7 | 9.6 | 11.0 | 8 | 9(>9溶解) |
(1)写出流程中第2次使用H2O2时,发生反应的离子方程式 。
(2)“调pH=8”和“调pH>11”中间的“过滤”步骤能否省略,为什么? 。
(3)流程图中从Na2CrO4溶液至产品中间“□”内的操作是 。
(4)CrO42-在酸性条件下转化为Cr2O72-。工业上常用Fe2+处理酸性K2Cr2O7废水,先将Cr2O72-转化为Cr3+,该反应的离子方程式为 ,再调节溶液的pH= ,使金属离子生成沉淀而除去。
Ⅱ(4分)(1)已知:20°C时,H2CO3:Ka1=4.2×10ˉ7、Ka2=5.6×10ˉ11;NH3•H2O:Kb=1.7×10ˉ5,碳酸氢铵溶液中HCO3ˉ、NH4+、OHˉ、H+四种离子浓度由大到小的顺序为
(2)羟胺(NH2OH)可看做是氨分子内的1个氢原子被羟基取代的物质,常用作还原剂.可以除去含Fe2+中的Fe3+,氧化产物是一种性质稳定、无污染的气体,写出反应的离子方程式 .
为提纯下列物质(括号内为杂质),选用的试剂或方法有错误的是
物质 | 试剂 | 分离方法 | |
A | 硝酸钾(氯化钠 ) | 蒸馏水 | 降温结晶 |
B | 氢氧化铁胶体(Fe3+) | 蒸馏水 | 渗析 |
C | 甲烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
D | 乙醇(水) | 生石灰 | 蒸馏 |