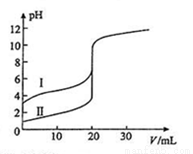
已知25℃时有关弱电解质的电离平衡常数如下表:
弱电解质化学式 | CH3COOH | HCN | H2CO3 | NH3.H2O |
电离平衡常数 | 1.8×l0–5 | 4.9×l0–10 | K1=4.3×l0–7 K2=5.6×l0–11 | 1.8×l0–5 |
根据上表中数据回答下列问题:
(1)CH3COO- 、CN- 、CO32-结合质子(即H+)的能力大小顺序__________________;25℃时,有等浓度的①CH3COONa溶液、②NaCN溶液、③NaHCO3溶液,三种溶液的pH由大到小的顺序为 (填序号)。
(2)NaCN溶液中通入少量二氧化碳,反应的离子方程式为
(3)向稀氨水中加入等体积等浓度的醋酸溶液,则反应后溶液中各离子浓度大小关系为
(4)甲、乙两瓶氨水的浓度分别为1mol·L-1、0.1mol·L-1,则c(OH-)甲﹕c(OH-)乙 10(填“>”、“=”或“<”)。
(1)常温下将0.2 mol•L?1 HCl溶液与0.2 mol•L?1 MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,试回答以下问题:
①混合溶液中由水电离出的c(H+) 0.2 mol•L?1HCl溶液中由水电离出的c(H+);(填“>”、“<”、或“=”)
②混合溶液中c(Cl-)-c(M+)= mol•L?1。(填精确计算结果)
(2)常温下若将0.2 mol•L?1 MOH溶液与0.1 mol•L?1 HCl溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下MOH的电离程度 MCl的水解程度。(填“>”、“<”、或“=”)
(3)常温下若将pH=3的HR溶液与pH=11的NaOH溶液等体积混合,若溶液的pH不等于7,则混合溶液的pH 。(填“>7”、“<7”、或“无法确定”)
(4)用0.1000 mol•L?1 HCl溶液滴定未知浓度的NaOH溶液,重复三次的实验数据如下所示
实验序号 | 0.1000 mol•L?1 HCl溶液体积/mL | 待测NaOH溶液体积/mL |
1 | 27.83 | 20.00 |
2 | 25.53 | 20.00 |
3 | 27.85 | 20.00 |
①待测NaOH溶液的物质的量浓度为 mol•L?1。(保留四位有效数字)
②下列情况可能引起测定结果偏高的是 。
A.酸式滴定管未用标准盐酸溶液润洗
B.锥形瓶未用待测液润洗
C.到达滴定终点时,仰视读数
D.滴定前,滴定管中的溶液液面最低点在“0”点以下