一定温度下,在三个体积均为2.5L的恒容密闭容器中发生反应:
CO2(g)+H2S(g) 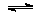 COS(g)+H2O(g)
COS(g)+H2O(g)
容器 | 温度/K | 起始物质的量/mol | 平衡物质的量/mol | 平衡常数 | |
CO2 | H2S | H2O | |||
Ⅰ | 607 | 0.11 | 0.41 | 0.01 | / |
Ⅱ | 607 | 0.22 | 0.82 | / | |
Ⅲ | 620 | 0.1 | 0.4 | / | 6.74×10-3 |
下列说法正确的是
A.该反应正反应为放热反应
B.607K时该反应的平衡常数为2.50×10-3
C.容器Ⅱ达到平衡时容器中COS的物质的量为0.02mol
D.容器Ⅲ达平衡时,再充入少量氦气,平衡将向正反应方向移动
 H>0,
H>0,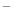 )
)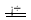 Na2S2O5 + H2O……(c)
Na2S2O5 + H2O……(c)
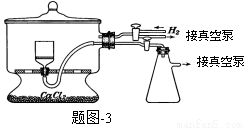
 慢变化,溶液开始逐渐变黄。“温度迅速升高”的原因为 ;
慢变化,溶液开始逐渐变黄。“温度迅速升高”的原因为 ;

 ③
③