某化工厂冶炼金属、回收硫的工艺流程如下:

I.回收硫
(1)工业上,采用饱和亚硫酸钠溶液吸收烟气中二氧化硫,写出离子方程式: 。然后,加热吸收液收集SO2。将二氧化硫、空气在稀硫酸中构成原电池,负极反应式为 。
II.冶炼铜
(2)工业上,火法冶炼铜分两步:第一步,含铜矿(主要成分是Cu2S)在空气中煅烧生成氧化亚铜和刺激性气味气体;第二步,氧化亚铜和铜矿在高温下反应生成铜和刺激性气体。写出冶炼铜的总反应方程式: 。
(3)用电解法精炼粗铜(含银、金、铁、锌杂质),装置如图所示。下列说法不正确的是 。
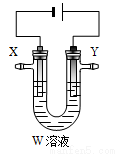
A.Y极为粗铜、X极为纯铜
B.X极净增质量等于Y极净减质量
C.铜盐溶液作精炼铜的电解质溶液
D.若电路有1 mol电子转移,则X极净增32 g
(4)几种金属离子的沉淀pH:
金属氢氧化物 | 开始沉淀pH | 完全沉淀的pH |
Fe(OH)3 | 2.7 | 3.7 |
Fe(OH)2 | 7.6 | 9.7 |
Cu(OH)2 | 4.6 | 6.4 |
Zn(OH)2 | 5.9 | 8.9 |
铜盐溶液中Fe2、Zn2+对精炼铜可能会产生影响。工业上,除去Fe2+方法是,在酸性混合溶液中加入 (选填:双氧水、次氯酸钠、氯水或高锰酸钾溶液)将Fe2+氧化成Fe3+,离子方程式为 。加入碱调节溶液pH范围为 。
下表中列出了五种短周期元素A、B、C、D、E的信息,请推断后作答:
元素 | 有关信息 |
A | 元素主要化合价为-2,原子半径为0.074nm |
B | 所在主族序数与所在周期序数之差为4,同周期主族元素中原子半径最小 |
C | 原子半径为0.102nm,其单质在A的单质中燃烧,发出明亮的蓝紫色火焰 |
D | 最高价氧化物对应水化物,能按1:1电离出电子数相等(10个电子)的阴阳离子 |
E | 原子半径为0.075nm,最高价氧化物对应水化物与其氢化物组成一种盐X |
(1)写出A、E两种元素符号 、 。
(2)画出B原子的核外电子排布式: ;写出D元素最高价氧化物对应水化物的电子式: 。
(3)盐X水溶液显 (选填“酸”、“碱”或“中”)性,用离子方程式解释其原因: 。
(4)D2CA3的溶液与B的单质能发生氧化还原反应,其反应的离子方程式为 。
(5)已知E元素的某种氢化物Y与A2的摩尔质量相同,Y在常温下为液态,Y的化学式为 ,Y所含的化学键为 。
(a)极性键 (b)非极性键 (c)离子键


