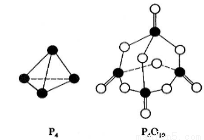
相同温度下,容积相同的甲、乙、丙3个恒容密闭容器中发生可逆 反应:2SO2(g)+O2(g)
反应:2SO2(g)+O2(g) 2SO3(g)△H = -197kJ/mol。实验测得起始、平衡时的有关数据如右表所示。下列叙述正确的是
2SO3(g)△H = -197kJ/mol。实验测得起始、平衡时的有关数据如右表所示。下列叙述正确的是
容器 | 起始各物质的物质的量/mol | 达到平衡时体 系能量的变化 | |||
SO2 | O2 | SO3 | Ar | ||
甲 | 2 | 1 | 0 | 0 | 放出热量:Q1 |
乙 | 1.8 | 0.9 | 0.2 | 0 | 放出热量:Q2 |
丙 | 1.8 | 0.9 | 0.2 | 0.1 | 放出热量:Q3 |
A.Q1=Q2=Q3
B.达到平衡时,丙容器中SO2的体积分数最大
C.甲、乙、丙3个容器中反应的平衡常数不相等
D.若在上述条件下反应生成2molSO3(s)的放热大于197kJ
卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子。以卤块为原料可制得轻质氧化镁,工艺流程如图:

已知:Fe2+氢氧化物呈絮状,不易从溶液中除去,所以常将它氧化为Fe3+,生成Fe(OH)3沉淀除去。若要求产品尽量不含杂质,请根据表1和表2提供的资料,填写空白:
表1 生成氢氧化物沉淀的pH | 表2 化学试剂价格表 | ||||
物质 | 开始沉淀 | 沉淀完全 | 试剂 | 价格(元/吨) | |
Fe(OH)3 | 2.7 | 3.7 | 漂液(含25.2% NaClO) | 450 | |
Fe(OH)2 | 7.6 | 9.6 | 双氧水(含30% H2O2) | 2400 | |
Mn(OH)2 | 8.3 | 9.8 | 烧碱(含98% NaOH) | 2100 | |
Mg(OH)2 | 10.0 | 11.1 | 纯碱(含99.5% Na2CO3) | 600 | |
(1)在步骤②中加入的试剂X(从表2中选择)是___而不是双氧水,其原因是________________。
写出加入X发生反应的离子方程式_______________________________。
(2)在步骤③中控制pH=9.8,其目的是_______________________________。
(3)沉淀物A的成分为_____________,试剂Y(从表2中选择)应该是________。
(4)在步骤⑤中发生反应的化学方程式是_______________________________。
(5)若在实验室中完成步骤⑥,则沉淀物C必需在______(填仪器名称)中灼烧。
化学实验是学习化学的基础,要通过实验去学习化学。
(1)下列关于实验的叙述中正确的有________。
A.不慎碰翻燃着的酒精灯使酒精在桌面上燃烧起来,应立即用湿抺布灭火
B.不慎将酸沾到皮肤或衣物上,应立即用浓NaOH溶液清洗
C.用托盘天平称量物品质量时,物品应置于右盘
D.实验时应节约药品,实验剩余的药品应放回原试剂瓶
E.可燃性气体点燃前一定要验纯
F.使用分液漏斗前必须检查其是否漏水
(2)请将下列错误实验操作可能会引起的不良后果填在表格中。
实验 | 向试管中加锌粒 | 对量筒中液体读数 | 浓硫酸的稀释 |
错误操作 |
|
|
|
不良后果 |