0 147327 147335 147341 147345 147351 147353 147357 147363 147365 147371 147377 147381 147383 147387 147393 147395 147401 147405 147407 147411 147413 147417 147419 147421 147422 147423 147425 147426 147427 147429 147431 147435 147437 147441 147443 147447 147453 147455 147461 147465 147467 147471 147477 147483 147485 147491 147495 147497 147503 147507 147513 147521 203614
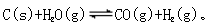 CO 的平衡物质的量浓
CO 的平衡物质的量浓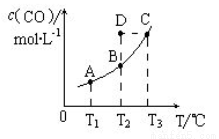

 2Z(g)
2Z(g)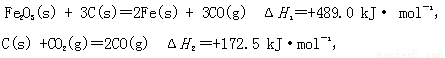
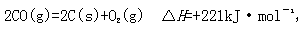 ,简述该设想能否实现的依据: 。
,简述该设想能否实现的依据: 。