室温下,将0.05 mol Na2CO3固体溶于水配成100mL溶液,向溶液中加入下列物质,有关结论正确的是
加入的物质 | 结论 | |
A | 50mL 1 mol·L-1H2SO4 | 反应结束后,c(Na+)=c(SO42-) |
B | 0.05molCaO | 溶液中 |
C | 50mL H2O | 由水电离出的c(H+)·c(OH—)不变 |
D | 0.1mol NaHSO4固体 | 反应完全后,溶液pH减小,c(Na+)不变 |
分析下表,下列选项中错误的是
化学式 | NH3·H2O | CH3COOH | HCN | H2CO3 |
电离平衡常数(25℃) | 1.8×l0—5 | 1.8×l0—5 | 4.9×l0—10 | K1= 4.3×l0—7, K2= 5.6×l0—11 |
A.0.1mol·L-1 CH3COONa 溶液显碱性,0.1mol·L-1 CH3COONH4 溶液显中性
B.等物质的量浓度的NaHCO3和NaCN溶液,前者溶液中水的电离程度大
C.NaCN + H2O + CO2 (少量) = HCN + NaHCO3
D.上述3种等体积等pH的酸溶液,分别加水稀释后pH仍相等,则醋酸中加入水的体积最少
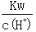 =1×10-13mol·L-1的溶液中:NH4+、Ca2+、Cl-、NO3-
=1×10-13mol·L-1的溶液中:NH4+、Ca2+、Cl-、NO3- Si(s)+4HCl(g);△H=+Q kJ·mol-1(Q>0)。某温度、压强下,将一定量的反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是
Si(s)+4HCl(g);△H=+Q kJ·mol-1(Q>0)。某温度、压强下,将一定量的反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是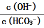 增大
增大
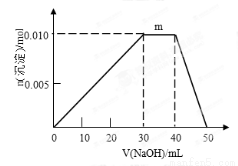
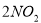

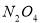 (正反应放热)。把烧瓶置于100℃的水中,则下列几项性质中不会改变的是( )
(正反应放热)。把烧瓶置于100℃的水中,则下列几项性质中不会改变的是( ) C(g)+3D(g),现从两条途径分别建立平衡。途径Ⅰ:A、B的起始浓度均为2mol/L;Ⅱ途径:C、D的起始浓度分别为2mol/L和6mol/L。以下叙述正确的是 ( )
C(g)+3D(g),现从两条途径分别建立平衡。途径Ⅰ:A、B的起始浓度均为2mol/L;Ⅱ途径:C、D的起始浓度分别为2mol/L和6mol/L。以下叙述正确的是 ( )