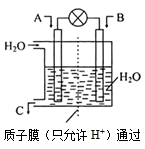
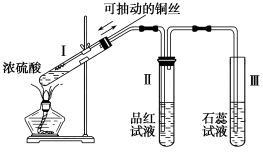
用试纸检验气体性质是一种重要的实验方法。如图所示的实验中(可加热),下列试纸的选用、现象及对应结论都正确的一项是

选项 | 试剂B | 湿润的试纸A | 现象 | 结论 |
A | 碘水 | 淀粉试纸 | 变蓝 | 碘具有氧化性 |
B | 浓氨水,生石灰 | 蓝色石蕊试纸 | 变红 | 氨气为碱性气体 |
C | Na2SO3,硫酸 | 品红试纸 | 褪色 | SO2具有漂白性 |
D | Cu,浓硝酸 | 淀粉KI试纸 | 变蓝 | NO2为酸性气体 |
常温下,有关下列4种溶液的说法正确的是
① | ② | ③ | ④ |
0.1 mol·L-1氨水 | pH=11 氨水 | 0.1 mol·L-1盐酸 | pH=3 盐酸 |
A.由水电离出的c(H+):③>①
B.①稀释到原来的100倍,pH与②相同
C.①与③混合,若溶液pH=7,则溶液中c(NH4+)>c(Cl-)
D.②与④等体积混合,混合液pH>7
向四支试管中分别加入少量不同的无色溶液进行如下操作,有关结论正确的是
选项 | 操作 | 现象 | 结论 |
A | 滴加氯水和CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
B | 向溶液X中先滴加稀硝酸, 再滴加BaCl2溶液 | 出现白色沉淀 | 溶液X中一定含有SO42- |
C | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰未呈紫色 | 原溶液中一定无K+ |
D | 滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |


 COCl2(g)制备。左图为此反应的反应速率随温度变化的曲线,右图为某次模拟实验研究过程中固定体积容器内各物质的浓度随时间变化的曲线。回答下列问题:
COCl2(g)制备。左图为此反应的反应速率随温度变化的曲线,右图为某次模拟实验研究过程中固定体积容器内各物质的浓度随时间变化的曲线。回答下列问题:
 CH3OH+H2O
CH3OH+H2O