根据表中信息判断,下列选项正确的是
序号 | 反应物 | 产物 |
① | KMnO4、H2O2、H2SO4 | K2SO4…… |
② | C12、FeBr2 | FeC13、FeBr3 |
③ | MnO4-…… | C12、Mn2+…… |
A.第①组反应的其余产物为H2O、MnSO4
B.第②组反应中Cl2与FeBr2的物质的量之比小于或等于1:2
C.第③组反应中生成lmol Cl2,转移电子5mol
D.氧化性由强到弱顺序为MnO4一>Cl2> Fe3+> Br2
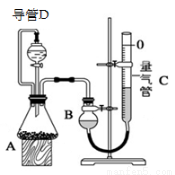
某探究性学习小组设计如右图所示装置分别进行如下探究实验,请回答下列问题:
实验 | 药品 | 制取气体 | 量气管中的液体 |
Ⅰ | Cu、稀HNO3 | H2O | |
Ⅱ | NaOH固体、浓氨水 | NH3 | |
Ⅲ | 镁铝合金、足量NaOH溶液 | H2 | H2O |
(1)实验I通过收集并测量NO气体的体积来探究铜样品的纯度,有的同学认为该实验设计不可行,主要原因是 ;
(2)实验Ⅱ中量气管中的液体最好是 (填字母编号, 下同)
A.NaOH溶液 B.氨水 C.煤油 D.氯化铵溶液
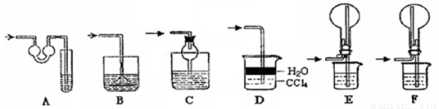
实验剩余的NH3需吸收处理,以下各种尾气吸收装置中,不能防止倒吸的是 ;
(3)①写出实验Ⅲ中涉及的离子反应方程式 ;
②反应前,先对量气管进行第一次读数。读数时,应注意的操作是 ,并使视线与凹液面最低处相平;反应后,待装置温度冷却到室温时,再对量气管进行第二次读数。实验前,如拆去导管D,测得的气体体积将 (填“偏大”、“偏小”、或“无影响”)。
③实验Ⅲ在25℃、1.01×105Pa条件下获得以下数据:
编号 | 镁铝合金质量 | 量气管第一次读数 | 量气管第二次读数 |
① | 1.0g | 10.0mL | 376.6mL |
② | 1.0g | 10.0mL | 364.7mL |
③ | 1.0g | 10.0mL | 377.0mL |
根据上述数据,计算出镁铝合金中铝的质量分数为 。
 的溶液中:ClO-、Cl-、K+、HSO3-
的溶液中:ClO-、Cl-、K+、HSO3-



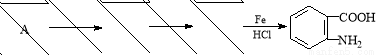
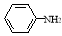 )易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位。据此按先后顺序写出以A为原料合成邻氨基苯甲酸(
)易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位。据此按先后顺序写出以A为原料合成邻氨基苯甲酸(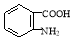 )合成路线中两种中间产物的结构简式(部分反应条件已略去) 。
)合成路线中两种中间产物的结构简式(部分反应条件已略去) 。