用碳酸钙与1mol/L稀盐酸反应制取二氧化碳,下列措施对化学反应速率几乎没有影响的是( )
|
| A. | 改用浓度为0.5mol/L的稀硫酸 |
|
| B. | 加入更多的碳酸钙 |
|
| C. | 稍微加热,升高反应温度 |
|
| D. | 加入少量醋酸钠晶体 |
下列实验事实与平衡移动无关的是( )
|
| A. | 氯气难溶于饱和食盐水 |
|
| B. | 用加压的方法促进CO2在水中的溶解 |
|
| C. | FeCl3+3KSCN⇌Fe(SCN)3+KCl,向体系中加入KCl固体 |
|
| D. | 合成氨工业中,及时将氨气液化移出 |
下列方法中可以说明2HI(g)⇌H2(g)+I2(g)已达到平衡的是( )
|
| A. | c(HI):c(H2):c(I2)=2:1:1时 |
|
| B. | 温度和体积一定时,混合气体的颜色不再改变 |
|
| C. | 单位时间内生成n mol H2的同时消耗2n mol HI |
|
| D. | 温度和体积一定时,容器内压强不再变化 |
右图是某太空空间站能量转化系统的局部示意图,基中燃料电池采用KOH为电解液,下列有关说法中正确的是( )

|
| A. | 该能量转化系统工作时,需不断补充H2O |
|
| B. | 该转化系统的能量本质上来源于太阳能 |
|
| C. | 水电解系统中的阴极反应:4OH﹣﹣4e﹣=O2+2H2O |
|
| D. | 燃料电池放电时的负极反应:H2﹣2e﹣=2H+ |
下列四种装置(电解质溶液皆为海水)中的铁电极腐蚀速率从快到慢顺序为( )
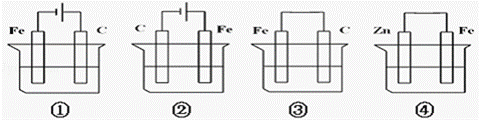
|
| A. | ②③④① | B. | ②③①④ | C. | ①④③② | D. | ①②③④ |
下列关于热化学的说法正确的是( )
|
| A. | 需要加热才能发生的反应是吸热反应 |
|
| B. | 等量的金刚石和石墨固体分别完全燃烧,前者放出热量多,说明金刚石更稳定 |
|
| C. | 化学反应的反应热只与反应体系的始态和终点状态有关,而与反应的途径无关 |
|
| D. | 由热化学方程式 3H2(g)+N2(g)⇌2NH3(g)△H=﹣92 kJ/mol可知,1molN2与3molH2放入密闭容器中,在催化剂的作用下反应得到氨气,将释放92kJ热量 |
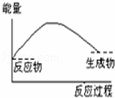
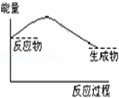
下列反应△H<0的是( )
|
| A. | 、 | B. |
| C. |
| D. | 、 |
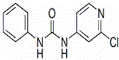
西瓜膨大剂别名氯吡苯脲,是经过国家批准的植物生长调节剂,实践证明长期使用对人体无害.已知其相关性质如下表所示:
| 分子式 | 结构简式 | 外观 | 熔点 | 溶解性 |
| C12H10ClN3O |
| 白色结晶粉末 | 170~172°C | 易溶于水 |
(1)氯元素基态原子核外电子的成对电子数为 .
(2)氯吡苯脲的晶体类型为 ,所含第二周期元素第一电离能从大到小的顺序为 N .
(3)氯吡苯脲晶体中,氮原子的杂化轨道类型为 .
(4)氯吡苯脲晶体中,微粒间的作用力类型有 .
A.离子键 B.金属键 C.共价键 D.配位键 E.氢键
(5)氯吡苯脲熔点低,易溶于水的原因分别为
(6)查文献可知,可用2﹣氯﹣4﹣氨基吡啶与异氰酸苯酯反应,生成氯吡苯脲.
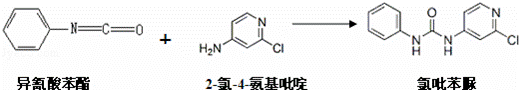
反应过程中,每生成1mol氯吡苯脲,断裂 个σ键、断裂 个π键.
原子序数依次增加的A、B、C、D、E、F六种常见元素中,A、B、C、D是短周期非金属元素,B、C、D同周期,E、F是第四周期的金属元素,F+的三个能层电子全充满.下表是主要化合价及原子半径数据:
| A | B | C | D | E | F | |
| 主要化合价 | ﹣1 | ﹣3+5 | ﹣2+6 | ﹣1+7 | +2 | +1+2 |
| 原子半径 | 0.071 | 0.11 | 0.102 | 0.099 | 0.197 | 0.117 |
(1)B、C、D三种元素第一电离能数值由小到大的顺序是 (填元素符号);
(2)B的氢化物中心原子采取 杂化,空间构型是 形,是 分子(填“极性”或“非极性”);
(3)F2+与NH3形成配离子的结构式为 + ;往某种蓝色溶液中加入氨水,形成蓝色沉淀,继续加入氨水,难溶物溶解变成蓝色透明溶液,可得到含有上述配离子的配合物.写出沉淀溶解的离子方程式 .
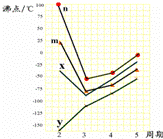
(4)A、E两种元素形成晶体晶胞是图中的 (填①、②、③或④);
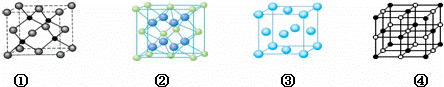
(5)如图四条折线分别表示ⅣA族、ⅤA族、ⅥA族、ⅦA族元素气态氢化物沸点变化,请选出C的氢化物所在的折线 (填n、m、x或y).