有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请回答问题.
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第八列 |
(1)已知BA5为离子化合物,是由 、 两种微粒构成的(填化学符号).
(2)B基态原子中能量最高的电子,其电子云在空间有 个方向,原子轨道呈 形.
(3)某同学根据上述信息,推断C基态原子的核外电子排布为,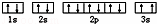 该同学所画的电子排布图违背了 .
该同学所画的电子排布图违背了 .
(4)G位于 族,G3+价电子排布式为 .GE3常温下为固体,熔点282℃,沸点315℃,在300℃以上升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂.据此判断GE3的晶体类型为 .
(5)DE3中心原子的杂化方式为 ,其空间构型为 .
(6)前四周期中与F同一族的所有元素分别与E元素形成化合物,其晶体的熔点由高到低的排列顺序为(写化学式) ,原因是 .
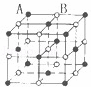
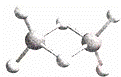
近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧时放出大量的热量.Al2H6球棍模型如图.下列说法肯定错误的是( )
|
| A. | Al2H6在固态时所形成的晶体是分子晶体 |
|
| B. | 氢铝化合物可能成为未来的储氢材料和火箭燃料 |
|
| C. | Al2H6在空气中完全燃烧,产物为氧化铝和水 |
|
| D. | Al2H6中含有离子键和极性共价键 |
有关晶体的下列说法中不正确的是( )
|
| A. | 在NaCl晶体中,距Na+最近的Cl﹣形成正八面体 |
|
| B. | 在NaCl晶体中,每个晶胞平均占有4个Na+ |
|
| C. | 在CsCl晶体中,每个晶胞平均占有8个Cs+ |
|
| D. | 铜晶体为面心立方堆积,铜原子的配位数(距离一个铜原子最近的其它铜原子的个数)为12 |
下列对一些实验事实的理论解释正确的是( )
| 选项 | 实验事实 | 理论解释 |
| A | 氮原子的第一电离能大于氧原子 | 氮原子2p能级半充满 |
| B | CO2为直线形分子 | CO2分子为非极性分子 |
| C | 金刚石的熔点低于石墨 | 石墨熔融时除了破坏共价键,还需破坏范德华力 |
| D | HF的沸点高于HCl | H﹣F的键能大于H﹣Cl |
|
| A. | A | B. | B | C. | C | D. | D |