某烯烃与氢气加成后得到2,2﹣二甲基丁烷,则该烯烃的名称是( )
|
| A. | 3,3﹣二甲基﹣1﹣丁烯 | B. | 2,2﹣二甲基﹣2﹣丁烯 |
|
| C. | 2,2﹣二甲基﹣1﹣丁烯 | D. | 2,2﹣二甲基﹣3﹣丁烯 |
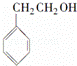
下列物质中既属于芳香族化合物又属于醇的是( )
|
| A. |
| B. |
| C. |
| D. | CH3CH2OH |
金属冶炼和处理常涉及氧化还原反应。
(1)由下列物质冶炼相应金属时采用电解法的是
a.Fe2O3 b.MgCl2 c.Cu2S d.Ag2O
(2)钢铁是21世纪用途最广的结构材料和功能材料。工业上在炼铁高炉中用CO热还原Fe2O3冶炼铁。写出该反应的化学方程式并用单线桥表示电子转移的方向和数目。
|
(3)辉铜矿(Cu2S)可发生反应2Cu2S+3O2======2Cu2O+2SO2,该反应的氧化产物是 ,当1mol O2发生反应时,还原剂所失电子的物质的量为 mol。煅烧2.0t含80%Cu2S的辉铜矿石(杂质不参加反应)时,若SO2 的利用率为94%,可生产质量分数为98%的硫酸的质量为 t。(4分)
已知A(g)  B(g)+C(g)反应的平衡常数和温度的关系如下:
B(g)+C(g)反应的平衡常数和温度的关系如下:
| 温度/ ℃ | 700 | 800 | 900 | 1000 |
| 平衡常数 | 0.4 | 0.9 | 1.0 | 1.6 |
回答下列问题:
(1)该反应的平衡常数表达式K= ,△H 0,△S 0(填“<”“ >”“ =”)
(2)900℃时,向一个0.5 L的密闭容器中充入6mol的A,如反应初始5s内A的平均反应速率v(A)=0.4 mol·L-1·s-1。则5s时c(A)= mol·L-1, C的物质的量为 mol;若反应经一段时间后,达到平衡时A的转化率为 。保持温度和体积不变,再向容器中充入4mol的A,则重新达到平衡时A的转化率为
(3)700℃时反应C(g)+B(g) A(g)的平衡常数的值为
A(g)的平衡常数的值为
在一定温度下,将气体X和气体Y各0. 16 mol充入2 L恒容密闭容器中,发生反应
X(g)+Y(g)=2Z(g) ,一段时间后达到平衡。反应过程中测定的数据如下表:
| t/min | 2 | 4 | 7 | 9 |
| n(X)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是( )
A、反应前2 min的平均速率ν(Z)=0.04mol/(L·min)
B.保持其他条件不变,若升高温度,平衡时c(X)= 0.06 mol·L-1,则该反应的H>0
C.相同温度下,起始时向容器中充入1mol X、0.2mol Y 和0.2mol Z,反应达到平衡前v(正)>v(逆)
D、其他条件不变,从反应体系中移走一部分 Z,正反应速率增大,逆反应速率减小,平衡正向移动
用右图所示装置检验乙烯时不需要除杂的是
| 乙烯的制备 | 试剂X | 试剂Y | |
| A | CH3CH2Br与NaOH乙醇溶液共热 | H2O | KMnO4酸性溶液 |
| B | CH3CH2Br与NaOH乙醇溶液共热 | H2O | Br2的CCl4溶液 |
| C | CH3CH2OH与浓H2SO4加热至170℃ | NaOH溶液 | KMnO4酸性溶液 |
| D | CH3CH2OH与浓H2SO4加热至170℃ | NaOH溶液 | Br2的CCl4溶液 |

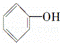
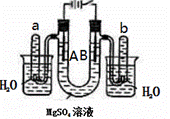 (5)电解一段时间后,切断电源,将电解液导入烧杯内观察到的现象是__________________.
(5)电解一段时间后,切断电源,将电解液导入烧杯内观察到的现象是__________________.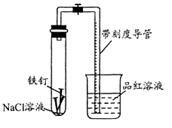 ③将导管口浸入品红溶液
③将导管口浸入品红溶液
 zC(g),达到平衡时,测得平衡时C的物质的量浓度为0.35 mol·L-1,保持温度不变,将容器容积压缩到原来的一半,再次达到平衡,测得C的物质的量浓度为0.6 mol·L-1,下列有关分析正确是
zC(g),达到平衡时,测得平衡时C的物质的量浓度为0.35 mol·L-1,保持温度不变,将容器容积压缩到原来的一半,再次达到平衡,测得C的物质的量浓度为0.6 mol·L-1,下列有关分析正确是