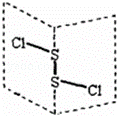
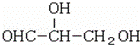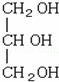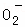二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下S2Cl2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体.下列说法错误的是( )
|
| A. | S2Cl2的结构式为Cl﹣S﹣S﹣Cl |
|
| B. | S2Cl2为含有极性键和非极性键的极性分子 |
|
| C. | S2Br2与S2Cl2结构相似,分子间作用力:S2Br2>S2Cl2 |
|
| D. | S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O═SO2↑+4HCl |
下列化合物中含有2个手性碳原子的是( )
|
| A. |
| B. |
| C. | CF2Cl2 | D. |
|
高温下,超氧化钾晶体呈立方体结构,晶体中氧的化合价部分为0价,部分为﹣2价.如图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元),则下列说法中正确的是( )

|
| A. | 超氧化钾的化学式为KO2,每个晶胞含有4个K+和4个 |
|
| B. | 晶体中每个K+周围有8个 |
|
| C. | 晶体中与每个K+距离最近的K+有8个 |
|
| D. | 晶体中,0价氧原子与﹣2价氧原子的数目比为3:1 |
关于晶体的自范性,下列叙述正确的是( )
|
| A. | 破损的晶体能够在固态时自动变成规则的多面体 |
|
| B. | 缺角的氯化钠晶体在饱和NaCl溶液中慢慢变为完美的立方体晶块 |
|
| C. | 圆形容器中结出的冰是圆形的体现了晶体的自范性 |
|
| D. | 由玻璃制成规则的玻璃球体现了晶体的自范性 |
某物质的实验式为PtCl4•2NH3,其水溶液不导电,加入AgNO3溶液反应也不产生沉淀,以强碱处理并没有NH3放出,则关于此化合物的说法中正确的是( )
|
| A. | 配合物中中心原子的电荷数和配位数均为6 |
|
| B. | 该配合物可能是平面正方形结构 |
|
| C. | Cl﹣ 和NH3分子均与Pt4+配位 |
|
| D. | 配合物中Cl﹣ 与Pt4+配位,而NH3分子不配位 |
根据等电子原理判断,下列说法中错误的是( )
|
| A. | B3N3H6分子中所有原子均在同一平面上 |
|
| B. | B3N3H6分子中存在双键,可发生加成反应 |
|
| C. | H3O+和NH3是等电子体,均为三角锥形 |
|
| D. | CH4和NH4+是等电子体,均为正四面体 |
已知SO3、BF3、CCl4、PCl5、SF6都是非极性分子,而H2S、NH3、NO2、SF4、BrF5都是极性分子,由此可推出ABn型分子属于非极性分子的经验规律是( )
|
| A. | ABn型分子中A、B均不含氢原子 |
|
| B. | A元素的相对原子质量必小于B元素的相对原子质量 |
|
| C. | 分子中所有原子都在同一平面上 |
|
| D. | ABn型的价层电子对数等于n |
R为1~18号元素,其原子所具有的电子层数为最外层电子数的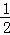 ,它可能形成的含氧酸根离子有:①R2O42﹣,②RO42﹣,③R2O32﹣,④RO32﹣,下列叙述判断正确的是( )
,它可能形成的含氧酸根离子有:①R2O42﹣,②RO42﹣,③R2O32﹣,④RO32﹣,下列叙述判断正确的是( )
|
| A. | 当它可以形成①时,不可能形成④ |
|
| B. | 当它可以形成②时,可以形成③和④ |
|
| C. | 当它可以形成①时,不可能形成②和③ |
|
| D. | 当它形成②时,也可以形成① |
下列叙述中,正确的是( )
|
| A. | 在一个基态多电子的原子中,可以有两个运动状态完全相同的电子 |
|
| B. | 在一个基态多电子的原子中,不可能有两个能量完全相同的电子 |
|
| C. | 在一个基态多电子的原子中,M层上的电子能量肯定比L层上的电子能量高 |
|
| D. | 如果某一基态3p能级上仅有2个电子,它们自旋方向必然相反 |