X、Y两元素的质子数之和为22,X的原子核外电子数比Y少6个,下列说法中不正确的是( )
|
| A. | Y的单质是金属晶体 |
|
| B. | X的单质固态时为分子晶体 |
|
| C. | X与碳形成的化合物为分子晶体 |
|
| D. | X与Y形成的化合物固态时为分子晶体 |
三氯化氮(NCl3)常温是一种淡黄色液体,其分子结构呈三角锥形,以下关于NCl3的说法中正确的是( )
|
| A. | 它是一种非极性分子 |
|
| B. | 它能以配位键与Cl﹣结合,生成NCl4﹣ |
|
| C. | NCl3中N原子采用SP2杂化 |
|
| D. | 已知NCl3中N元素为﹣3价,所以NCl3水解产物为NH3和HClO |
下列关于晶体说法的正确组合是( )
①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低
④离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
⑤CaTiO3晶体中(晶胞结构如图所示)每个Ti4+和12个O2﹣紧邻
⑥60gSi02中含Si﹣O键的个数为2NA
⑦晶体中分子间作用力越大,分子越稳定
⑧氯化钠熔化时离子键被破坏
⑨124g P4含有P﹣P键的个数为4NA.

|
| A. | ①②③⑥ | B. | ①②④ | C. | ③⑤⑦ | D. | ③⑤⑧ |
短周期元素W、X、Y、Z的原子序数依次增大,其中W的阴离子的核外电子数与X、Y、Z原子的核外内层电子数相同.X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,而Z不能形成双原子分子.根据以上叙述,下列说法中正确的是( )
|
| A. | 上述四种元素的原子半径大小为W<X<Y<Z |
|
| B. | W、X、Y、Z原子的核外最外层电子数的总和为20 |
|
| C. | W与Y可形成既含极性共价键又含非极性共价键的化合物 |
|
| D. | 由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点 |
下列说法不正确的是( )
|
| A. | 离子晶体的晶格能越大离子键越强 |
|
| B. | 阳离子的半径越大则可同时吸引的阴离子越多 |
|
| C. | 通常阴、阳离子的半径越小、电荷越大,该阴阳离子组成离子化合物的晶格能越大 |
|
| D. | 拆开1mol离子键所需的能量叫该离子晶体的晶格能 |
下列关于金属晶体的叙述正确的是( )
|
| A. | 常温下,金属单质都以金属晶体形式存在 |
|
| B. | 金属离子与自由电子之间的强烈作用,在一定外力作用下,不因变形而消失 |
|
| C. | 钙的熔沸点低于钾 |
|
| D. | 温度越高,金属的导电性越好 |
不能说明X的电负性比Y的大的是( )
|
| A. | 与H2化合时X单质比Y单质容易 |
|
| B. | X的最高价氧化物的水化物的酸性比Y的最高价氧化物的水化物的酸性强 |
|
| C. | X原子的最外层电子数比Y原子的最外层电子数多 |
|
| D. | X单质可以把Y从其氢化物中置换出来 |
下列叙述正确的是( )
|
| A. |
|
|
| B. | 不同元素的原子构成的分子只含极性共价键 |
|
| C. |
|
|
| D. | 短周期第ⅣA与ⅦA族元素的原子间构成的分子,均满足原子最外层8电子结构 |
关于原子轨道的说法正确的是( )
|
| A. | 凡是中心原子采取sp3杂化方式成键的分子其几何构型都是正四面体 |
|
| B. | CH4分子中的sp3杂化轨道是由4个H原子的1s轨道和C原子的2p轨道混合起来而形成的 |
|
| C. | sp3杂化轨道是由同一个原子中能量相近的s轨道和p轨道混合起来形成的一组能量相同的新轨道 |
|
| D. | 凡AB3型的共价化合物,其中心原子A均采用sp3杂化方式成键 |
下列各组元素中,第一电离能依次减小的是( )
|
| A. | H Li Na K | B. | Na Mg Al Si |
|
| C. | I Br Cl F | D. | F O N C |
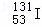 放出射线是一个自发的化学变化过程,射线对人危害很大
放出射线是一个自发的化学变化过程,射线对人危害很大 和
和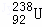 是中子数不同质子数相同的同种核素
是中子数不同质子数相同的同种核素