根据表提供的数据,判断在等浓度的NaClO、NaHCO3混合溶液中,各种离子浓度关系正确的是( )
| 化学式 | 电离常数 |
| HClO | K=3×10﹣8 |
| H2 CO3 | K1=4.3×10﹣7 |
| K2=5.6×10﹣11 |
|
| A. | c(HCO3﹣)>c(ClO﹣)>c(OH﹣) |
|
| B. | c(ClO﹣)>c(HCO3﹣)>c(H+) |
|
| C. | c(HClO)+c(ClO﹣)=c(HCO3﹣)+c(H2CO3﹣) |
|
| D. | c(Na+)+c(H+)=c(HCO3﹣)+c(ClO﹣)+c(OH﹣) |
已知室温时,0.1mol/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是( )
|
| A. | 该溶液的pH=4 |
|
| B. | 升高温度,溶液的pH增大 |
|
| C. | 此酸的电离平衡常数约为1×10﹣7 |
|
| D. | 由HA电离出的c(H+)约为水电离出的c(H+)的106倍 |
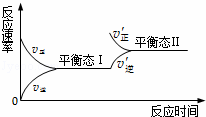
如图是恒温下某化学反应的反应速率随反应时间变化的示意图.下列叙述与示意图不相符合的是( )
|
| A. | 反应达平衡时,正反应速率和逆反应速率相等 |
|
| B. | 该反应达到平衡态Ⅰ后,增大反应物浓度,平衡发生移动,达到平衡态Ⅱ |
|
| C. | 该反应达到平衡态后,减小反应物浓度,平衡发生移动,达到平衡态Ⅱ |
|
| D. | 同一种反应物在平衡态Ⅰ和平衡Ⅱ时浓度不相等 |
反应4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g)在5L密闭容器中进行,半分钟后,水蒸气的物质的量增加了4.5mol,则此反应的平均速率 (反应物的消耗速率或产物的生成速率)可表示为( )
(反应物的消耗速率或产物的生成速率)可表示为( )
|
| A. | v(NH3)=0.01mol/(L•s) | B. | v(O2)=0.03mol/(L•s) |
|
| C. | v(NO)=0.02mol/(L•s) | D. | v(H2O)=0.04mol/(L•s) |
下列说法正确的是( )
|
| A. | AgCl水溶液中Ag+和Cl﹣浓度的乘积是一个常数 |
|
| B. | AgCl水溶液的导电性很弱,所以AgCl为弱电解质 |
|
| C. | 温度一定时,当AgCl水溶液中Ag+和Cl﹣浓度的乘积等于Ksp值时,此溶液为AgCl的饱和溶液 |
|
| D. | 向饱和AgCl水溶液中加入盐酸,c(Cl﹣)增大,Ksp值变大 |
已知当NH4Cl溶液的浓度小于0.1mol/L时,其pH>5.1.现用0.1mol/L的盐酸滴定10mL0.05mol/L的氨水,用甲基橙作指示剂达到终点时所用盐酸的量应是( )
|
| A. | 10mL | B. | 5mL | C. | 大于5mL | D. | 小于5mL |
下列溶液,一定呈中性的是( )
|
| A. | c(H+)=1×10﹣7mol/L的溶液 |
|
| B. | pH=pOH 的溶液 |
|
| C. | pH=14﹣pOH 的溶液 |
|
| D. | 由等体积、等物质的量浓度的一元酸跟氢氧化钠溶液混合后所形成的溶液 |
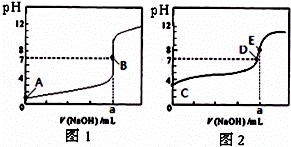
常温下,用0.1000mol/L NaOH溶液分别滴定20.00mL 0.1000mol/L 盐酸和20.00mL 0.1000mol/L 醋酸溶液,得到2条滴定曲线,如图所示.若以HA表示酸,下列说法正确的是( )
|
| A. | 滴定盐酸的曲线是图2 |
|
| B. | 达到B、D状态时,两溶液中离子浓度均为 c(Na+)=c(A﹣) |
|
| C. | 达到B、E状态时,反应消耗的n(CH3COOH)>n(HCl) |
|
| D. | 当0 mL<V(NaOH)<20.00 mL时,对应混合溶液中各离子浓度由大到小的顺序均为 c(A﹣)>c(Na+)>c(H+)>c(OH﹣) |
25℃时,有关弱酸的电离常数如下表,下列说法正确的是( )
| 弱酸 | CH3COOH | HCN | H2CO3 |
| Ka | 1.8×10﹣5 | 4.9×10﹣10 | K1:4.3×10﹣7 K2:5.6×10﹣11 |
|
| A. | 相等物质的量浓度溶液pH关系:pH (NaCN)>pH (Na2CO3)>pH (CH3COONa) |
|
| B. | 相等物质的量浓度的HCN和NaCN混合溶液中:c (HCN)+c(H+)=c (OH﹣)+c (CN﹣) |
|
| C. | a mol/LHCN与b mol/LNaOH溶液等体积混合后所得的溶液中:若c(Na+)>c (CN﹣),则a一定小于b |
|
| D. | 将Na2CO3加入到HCN溶液中时发生如下反应:Na2CO3+HCN=NaCN+NaHCO3 |