25℃时,水的电离可达到平衡:H2O⇌H++OH﹣△H>0,下列叙述正确的是( )
|
| A. | 向水中加入稀氨水,平衡逆向移动,c(OH﹣)降低 |
|
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
|
| C. | 向水中加入少量固体CH3COOH,平衡逆向移动,c(H+)降低 |
|
| D. | 将水加热,Kw增大,pH不变 |
以下有关溶液(均在常温下)的结论正确的是( )
|
| A. | pH=1的盐酸与pH=5的盐酸等体积混合后pH=3 |
|
| B. | 0.1mol/L醋酸溶液100 mL与0.2 mol/L氨水50 mL混合后能恰好完全中和 |
|
| C. | pH>7的溶液中不可能存在CH3COOH分子 |
|
| D. | 等浓度等体积的KOH溶液和CH3COOH溶液混合后:c(CH3COO﹣)=c(K+) |
下列各项中的两个量,其比值一定为2:1的是( )
|
| A. | 液面在“0”刻度时,50mL碱式滴定管和25mL碱式滴定管所盛液体的体积 |
|
| B. | 相同温度下,0.2mol•L﹣1醋酸溶液和0.1mol•L﹣1醋酸溶液中的c(H+) |
|
| C. | 在(NH4)2SO4溶液中,c(NH |
|
| D. | 相同温度下,等浓度的Ba(OH)2和NaOH溶液,前者与后者的c(OH﹣) |
某学生的实验报告所列出的下列数据中合理的是( )
|
| A. | 用10mL量筒量取7.13mL稀盐酸 |
|
| B. | 用托盘天平称量25.20g NaCl |
|
| C. | 用广泛pH试纸测得某溶液的pH为2.3 |
|
| D. | 用25mL滴定管做中和滴定时,用去某浓度的碱溶液21.70mL |
由水电离产生的c(H+)和c(OH﹣)的乘积为1×10﹣18的溶液里,可能大量共存的离子组( )
|
| A. | NH4+、Na+、Cl﹣、I﹣ | B. | Na+、K+、Fe3+、SCN﹣ |
|
| C. | Na+、Al3+、Cl﹣、AlO2﹣ | D. | Na+、K+、Cl﹣、HCO3﹣ |
当Mg(OH)2在水中达到溶解平衡时:Mg(OH)2(s)⇌Mg2+(aq)+2OH﹣(aq)要使Mg(OH)2进一步溶解,应向溶液中加少量的固体是( )
|
| A. | NH4Cl | B. | NaOH | C. | Na2CO3 | D. | Fe |
将0.2mol•L﹣1 HCN溶液和0.1mol•L﹣1的NaOH溶液等体积混合后,溶液显碱性,下列关系式中正确的是
( )
|
| A. | c(HCN)<c(CN﹣) | B. | c(Na+)<(CN﹣) |
|
| C. | c(HCN)﹣c(CN﹣)=c(OH﹣) | D. | c(HCN)+c(CN﹣)=0.1mol•L﹣1 |
有一支50mL酸式滴定管中盛盐酸,液面恰好在amL刻度处,把管内液体全部放出,盛入量筒内,所得液体体积一定是( )
|
| A. | a mL | B. | (50﹣a)mL | C. | 大于(50﹣a)mL | D. | 大于a mL |
某同学分析Zn与稀H2SO4的反应。
(1)该反应的离子方程式是 。
(2)制H2时,用稀硫酸而不用浓硫酸,原因是_________。
(3)已知:Zn(s)+1/2O2(g) ZnO(s) ΔH=-332 kJ/mol
ZnO(s) ΔH=-332 kJ/mol
ZnO(s) + H2SO4(aq)  ZnSO4(aq) + H2O(l) ΔH =-112kJ/mol
ZnSO4(aq) + H2O(l) ΔH =-112kJ/mol
H2(g) +1/2 O2(g) H2O(l) ΔH =-286kJ/mol
H2O(l) ΔH =-286kJ/mol
则Zn与稀H2SO4反应生成1mol H2 时的反应热ΔH = kJ/mol。
(4)该同学用如下装置进行实验,分析影响反应速率的因素。

实验时,从断开K开始,每间隔1分钟,交替断开或闭合K,并连续计数每1 分钟内从a管流出的水滴数,得到的水滴数如下表所示:
| 1分钟水滴数(断开K) | 34 | 59 | 86 | 117 | … | 102 |
| 1分钟水滴数(闭合K) | 58 | 81 | 112 | 139 | … | 78 |
分析反应过程中的水滴数,请回答:
①由水滴数58>34、81>59,说明在反应初期,闭合K时比断开K时的反应速率______(填“快”或“慢”),主要原因是_________。
②由水滴数102>78,说明在反应后期,断开K时的反应速率快于闭合K时的反应速率,主要原因是_________。
③ 从能量转换形式不同的角度,分析水滴数86>81、117>112的主要原因是_______。
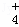 )与c(SO
)与c(SO )
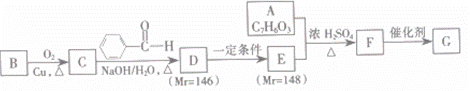
)
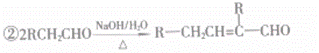
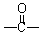 结构,②苯环上有2个取代基
结构,②苯环上有2个取代基