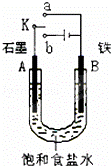
700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)⇌CO2+H2(g)反应过程中测定的部分数据见下表(表中t1>t2):
| 反应时间/min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
依据题意回答下列问题:
(1)反应在t1min内的平均速率为v(H2)= mol•L﹣1•min﹣1
(2)保持其他条件不变,起始时向容器中充入0.60molCO和1.20molH2O,到达平衡时,n(CO2)= mol.
(3)保持其他条件不变,向平衡体系中再通入0.20molH2O,与原平衡相比,达到新平衡时CO转化率 (填“增大”或“减小”或“不变”),H2O的体积分数 (填“增大”或“减小”或“不变”).
(4)温度升至800℃,上述反应平衡常数为0.64,则正反应为 反应(填“放热”或“吸热”).
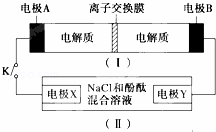
如图装置Ⅰ为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池充、放电的化学方程式为2K2S2+KI3 K2S2+3KI装置Ⅱ为电解池的示意图.当闭合开关K时,X附近溶液先变红,下列说法正确的是( )
K2S2+3KI装置Ⅱ为电解池的示意图.当闭合开关K时,X附近溶液先变红,下列说法正确的是( )
|
| A. | K+从右到左通过离子交换膜 |
|
| B. | 电极A的反应式:I3﹣+2e﹣=3I﹣ |
|
| C. | 电极X的反应式:4OH﹣﹣4e﹣═O2↑+2H2O |
|
| D. | 当电极Y有0.2mole﹣转移时,产生0.1molCl2 |
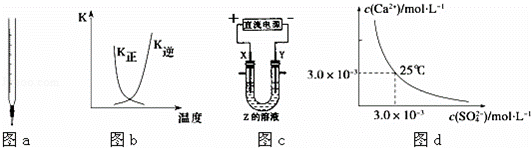
下列图示与对应的叙述相符的是( )
|
| A. | 图a为碱式滴定管,可盛装NaOH、KMnO4等溶液,不可盛装酸性液体 |
|
| B. | 图b中曲线表示反应2A(g)+B(g)⇌2C(g)△H>0,正、逆反应的平衡常数K随温度的变化 |
|
| C. | 图c表示铜的精炼,则X是精铜,Y是粗铜,Z是CuSO4溶液 |
|
| D. | 图d表示25℃时,CaSO4在水中的沉淀溶解平衡曲线.向100 mL该条件下的CaSO4饱和溶液中加入100 mL 0.01mol•L﹣1的Na2SO4溶液有沉淀析出 |
下列有关金属腐蚀与防护的说法正确的是( )
|
| A. | 纯银器表面在空气中因电化学腐蚀渐渐变暗 |
|
| B. | 当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
|
| C. | 在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
|
| D. | 可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
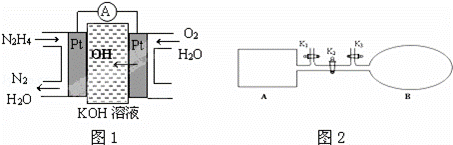
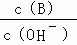 B.
B.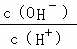 C.c (H+)•c (OH﹣) D.n (OH﹣)
C.c (H+)•c (OH﹣) D.n (OH﹣)