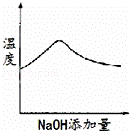
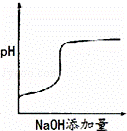
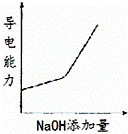
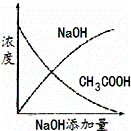
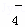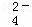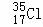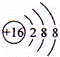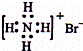已知某温度下纯水的pH=6,则该温度下0.05mol/L Ba(OH)2溶液的pH是( )
|
| A. | 13 | B. | 12.7 | C. | 11 | D. | 10.7 |
已知元素X的基态原子最外层电子排布为nsn﹣1npn+2,则它最高价氧化物对应的水化物的酸根离子是( )
|
| A. | RO | B. | RO43﹣ | C. | RO | D. | RO32﹣ |
下列有关化学用语使用不正确的是( )
|
| A. | 原子核内有18个中子的氯原子: |
|
| B. | S2﹣的结构示意图: |
|
| C. | 钒原子电子排布式:[Ar]3d34s2 |
|
| D. | NH4Br的电子式: |
用中和滴定法测定某烧碱样品的纯度,试根据实验回答下列问题:
(1)准确称量8.2g含有少量中性易溶杂质的样品,配成500mL待测溶液.称量时,样品可放在 (填编号字母)上称量
(A)小烧杯 (B)洁净纸片 (C)直接放在托盘上
(2)滴定时,用0.2000mol•L﹣1的盐酸来滴定待测溶液,不可选用 (填编号字母)作指示剂.
(A)甲基橙 (B)石蕊 (C)酚酞
(3)根据你所选择的指示剂,正确判断滴定终点的现象是: .
(4)根据下表数据,计算被测烧碱溶液的物质的量浓度是 mol•L﹣1,烧碱样品的纯度是 97.56% .
| 滴定次数 | 待测溶液体积(mL) | 标准酸体积 |
|
| 滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.00 | 4.10 | 24.00 |
(5)下列实验操作会对滴定结果产生的后果.(填“偏高”、“偏低”或“无影响”)
①观察酸式滴定管液面时,开始俯视,滴定终点平视,则滴定结果 .
②若将锥形瓶用待测液润洗,然后再加入10.00mL待测液,则滴定结果 .
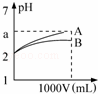
pH=2的A、B两种酸溶液各1mL,分别加水稀释到1L(其pH与溶液体积V的关系如图所示),下列说法正确的是( )
①a=5时,A是强酸,B是弱酸;
②若A、B都是弱酸,则5>a>2;
③稀释后,A酸溶液的酸性比B酸溶液强;
④A、B两种酸溶液的物质的量浓度一定相等.
|
| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |