下列各关系式中能说明反应N2+3H2⇌2NH3已达到平衡状态的是( )
|
| A. | 3υ正(N2)=υ正(H2) | B. | υ正(N2)=υ逆(NH3) |
|
| C. | υ正(N2)=3υ逆(H2) | D. | 2υ正(H2)=3υ逆(NH3) |
在不同条件下分别测得2SO2+O2⇌2SO3的化学反应速率,其中表示该反应进行最快的是( )
|
| A. | υ(SO2)=4 mol/(L•min) | B. | υ(O2)=0.1 mol/(L•s) |
|
| C. | υ(O2)=3mol/(L•min ) | D. | υ(SO2)=0.1 mol/(L•s) |
在一定条件下,CO和CH4燃烧的热化学方程式分别为
2CO(g)+O2(g)═2CO2(g)△H=﹣566kJ•mol﹣1
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890kJ•mol﹣1
由1mol CO(g)和3mol CH4(g)组成的混合气体在上述条件下充分燃烧,恢复至室温释放的热量为( )
|
| A. | 2912kJ | B. | 2953kJ | C. | 3236kJ | D. | 3867kJ |
下列热化学方程式中△H的绝对值能表示可燃物的燃烧热的是( )
|
| A. | H2(g)+Cl2(g)=2HCl(g);△H=﹣184.6kJ/mol |
|
| B. | CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=﹣802.3kJ/mol |
|
| C. | 2H2(g)+O2(g)=2H2O(l);△H=﹣571.6kJ/mol |
|
| D. | CO(g)+ |
14CO2与碳在高温条件下发生反应:14CO2+C⇌2CO,达到平衡后,平衡混合物中含14C的粒子有( )
|
| A. | 14CO2 | B. | 14CO2、14CO |
|
| C. | 14CO2、14CO、14C | D. | 14CO |
下列反应中生成物总能量高于反应物总能量的是( )
|
| A. | 碳酸钙受热分解 | B. | 乙醇燃烧 |
|
| C. | 铝与氧化铁粉未反应 | D. | 氧化钙溶于水 |
800℃时,在2L密闭容器中发生2NO(g)+O2(g)⇌2NO2(g),测得n(NO)随时间的变化如下表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.20 | 0.10 | 0.08 | 0.07 | 0.07 | 0.07 |
(1)用NO表示2s时该反应的平均速率v= mol•L﹣1•S﹣1
(2)写出该反应的平衡常数表达式:K= .
已知:K(800℃)>K(850℃),该反应是 (填“吸热”或“放热”)反应.
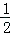 O2(g)=CO2(g);△H=﹣283kJ/mol
O2(g)=CO2(g);△H=﹣283kJ/mol