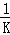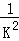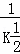有平衡体系CO(g)+2H2(g)═CH3OH(g)△H<0,为增加甲醇的产量,应采取的正确措施是( )
|
| A. | 高温、高压 | B. | 适宜的温度、高压、催化剂 |
|
| C. | 低温、高压、催化剂 | D. | 高温、高压、催化剂 |
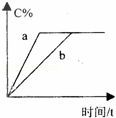
在a、b两个相同的容器中,分别加入相同量的A和B,发生可逆反应:A(g)+3B(g)⇌2C(g)(正反应为放热反应),两容器中C的体积分数与时间的关系如图所示,则a、b两线不同的可能原因是( )
|
| A. | a的温度高于b | B. | a使用了催化剂,而b未用 |
|
| C. | a的压强大于b | D. | a的温度低于b |
用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加大的是( )
|
| A. | 加热 |
|
| B. | 不用稀硫酸,改用98%的浓硫酸 |
|
| C. | 滴加少量CuSO4溶液 |
|
| D. | 不用铁片,改用铁粉 |
已知反应X+3Y2⇌Z+Q,在某段时间内以X的浓度变化表示的化学反应速度为1mol.L﹣1.min﹣1,则此段时间内以Z的浓度变化表示的化学反应速率为( )
|
| A. | 0.5mol•L﹣1•min﹣1 | B. | 1mol•L﹣1•min﹣1 |
|
| C. | 3mol•L﹣1•min﹣1 | D. | 2mol•L﹣1•min﹣1 |
气态PCl5的分解反应为2PCl5(g)⇌2PCl3(g)+2Cl2(g),在473K达到平衡时气态PCl5有48.5%分解,在573K达到平衡时气态PCl5有97%分解,则此反应是( )
|
| A. | 吸热反应 |
|
| B. | 放热反应 |
|
| C. | 反应的焓变为零的反应 |
|
| D. | 无法判断是吸热反应还是放热反应 |
下列关于化学平衡常数的说法中,正确的是( )
|
| A. | 在任何条件下,化学平衡常数都是一个定值 |
|
| B. | 当改变反应物的浓度时,化学平衡常数会发生改变 |
|
| C. | 化学平衡常数K只与温度、反应物浓度、体系的压强都有关 |
|
| D. | 化学平衡常数K可以推断一个可逆反应进行的程度 |
钢铁在空气中发生电化学腐蚀时,正极上发生的电极反应为( )
|
| A. | Fe﹣3 e﹣=Fe3+ | B. | 2H2O+O2+4e﹣=4OH﹣ |
|
| C. | Fe﹣2 e﹣=Fe2+ | D. | 4OH﹣﹣4e﹣=2H2O+O2↑ |
铁跟下列金属接触,能防止空气和水对铁腐蚀的是( )
|
| A. | 铜 | B. | 锌 | C. | 锡 | D. | 铅 |
 O2(g)⇌CO2(g)的平衡常数为K,则相同温度下反应2CO2(g)⇌2CO(g)+O2(g)的平衡常数K′为( )
O2(g)⇌CO2(g)的平衡常数为K,则相同温度下反应2CO2(g)⇌2CO(g)+O2(g)的平衡常数K′为( )