碱性电池具有容量大、放电电流大的特点,因而得到广泛应用.锌﹣锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)═Zn(OH)2(s)+Mn2O3(s),下列说法错误的是( )
|
| A. | 电池工作时,锌失去电子 |
|
| B. | 电池正极的电极反应式为:2MnO2(s)+H2O(l)+2e﹣═Mn2O3(s)+2OH﹣(aq) |
|
| C. | 电池工作时,电子由正极通过外电路流向负极 |
|
| D. | 外电路中每通过O.2mol电子,锌的质量理论上减小6.5g |
关于电解NaCl水溶液,下列叙述正确的是( )
|
| A. | 电解时在阳极得到氯气,在阴极得到金属钠 |
|
| B. | 若在阳极附近的溶液中滴入KI溶液,溶液呈棕色 |
|
| C. | 若在阴极附近的溶液中滴入酚酞试液,溶液呈无色 |
|
| D. | 电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后溶液呈中性 |
在铁制品上镀上一定厚度的锌层,以下设计方案正确的是( )
|
| A. | 锌作阳极,镀件作阴极,溶液中含有锌离子 |
|
| B. | 铂作阴极,镀件作阳极,溶液中含有锌离子 |
|
| C. | 铁作阳极,镀件作阴极,溶液中含有亚铁离子 |
|
| D. | 锌用阴极,镀件作阳极,溶液中含有锌离子 |
在电解水制取H2和O2时,为了增强导电性,常常要加入一些电解质,最好选用( )
|
| A. | NaOH | B. | HCl | C. | NaCl | D. | CuSO4 |
电解下列物质的水溶液时,在阴极区无金属析出的是( )
|
| A. | AgNO3 | B. | CuCl2 | C. | NaOH | D. | CaCl2 |
已知H2(g)+Cl2(g)═2HCl(g)△H=﹣184.6kJ/mol,则反应HCl(g)═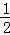 H2(g)+
H2(g)+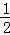 Cl2(g)的△H为( )
Cl2(g)的△H为( )
|
| A. | +184.6kJ/mol | B. | ﹣92.3kJ/mol | C. | ﹣369.2kJ/mol | D. | +92.3kJ/mol |
吸热反应一定是( )
|
| A. | 释放能量 |
|
| B. | 分解反应 |
|
| C. | 反应物的总能量低于生成物的总能量 |
|
| D. | 反应物的总能量高于生成物的总能量 |

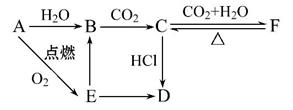
 C: ___________________________________________________,
C: ___________________________________________________,