在人类对原子结构认识道路上,根据α粒子散射现象,提出带核的原子结构模型的科学家是( )
|
| A. | 道尔顿 | B. | 爱因斯坦 | C. | 卢瑟福 | D. | 汤姆生 |
下列类型的反应,一定发生电子转移的是( )
|
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
某探究小组用KMnO4酸性溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素.实验条件作如下限定:所用KMnO4酸性溶液的浓度可选择0.01mol·L﹣1、0.001mol·L﹣1,催化剂的用量可选择0.5g、0g,实验温度可选择298K、323K.每次实验KMnO4酸性溶液的用量均为4mL、H2C2O4溶液(0.1mol·L﹣1)的用量均为2mL.
(1)配平化学方程式:
KMnO4+ H2C2O4+ H2SO4→ K2SO4+ MnSO4+ CO2+ H2O
(2)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
| 实验编号 | T/K | 催化剂的用量/g | KMnO4酸性溶液的浓度/mol·L﹣1 | 实验目的 |
| ① | 298 | 0.5 | 0.01 | (Ⅰ)实验①和②探究KMnO4酸性溶液的浓度对该反应速率的影响; (Ⅱ)实验①和③探究温度对该反应速率的影响; (Ⅲ)实验①和 ④ 探究催化剂对该反应速率的影响 |
| ② | ||||
| ③ | ||||
| ④ | 0 |
(3)在完成探究催化剂对该反应速率影响的实验时发现,未加催化剂的情况下,刚开始一段时间,反应速率较慢,溶液褪色不明显,但不久后突然褪色,反应速率明显加快.
针对上述实验现象,同学认为高锰酸钾与草酸溶液的反应放热,导致溶液温度升高,反应速率加快,从影响化学反应速率的因素看,你猜想还可能是
若用实验证明你的猜想.除酸性高锰酸钾溶液,草酸溶液外,还需要选择的试剂最合理的是
A.硫酸钾 B.硫酸锰 C.二氧化锰 D.水
(4)某同学对实验①和②分别进行三次实验,测得以下实验数据(从混合振荡均匀开始计时):
| KMnO4酸性溶液 的浓度/mol·L﹣1 | 溶液褪色所需时间 t/min | ||
| 第1次 | 第2次 | 第3次 | |
| 0.01 | 14 | 13 | 11 |
| 0.001 | 6 | 7 | 7 |
计算用0.001 mol·L﹣1 KMnO4酸性溶液进行实验时KMnO4的平均反应速率 (忽略混合前后溶液体积的变化).
(5)若不经过计算,直接看表中的褪色时间长短来判断浓度大小与反应速率的关系是否可行? .若不可行(若认为可行则不填),请设计可以通过直接观察褪色时间长短来判断的改进方案 .
在1LK2SO4和CuSO4的混合溶液中,c(SO42﹣)=2.0mol•L﹣1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L(标况)气体,则原溶液中K+的物质的量浓度为( )
|
| A. | 2.0mol•L﹣1 | B. | 1.5mol•L﹣1 | C. | 1.0mol•L﹣1 | D. | 0.5mol•L﹣1 |
在一体积不变的密闭容器中发生如下化学反应:2A(g)⇌B(g)+2C(g).当物质A的起始浓度为1.0mol•L﹣1、物质B、C的起始浓度为0时,物质A的浓度、转化率以及物质B的浓度随反应时间的变化如各图所示:
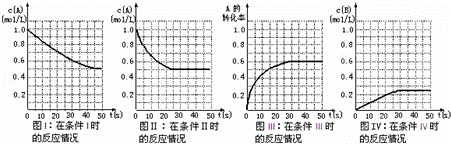
下列有关说法中正确的是( )
|
| A. | 条件Ⅰ、条件Ⅱ时的反应温度不同,压强相同 |
|
| B. | 条件Ⅰ时可能未使用催化剂,条件Ⅱ时可能使用了催化剂 |
|
| C. | 条件Ⅲ时的平衡混合物中,物质C的浓度等于0.6mol•L﹣1 |
|
| D. | 条件Ⅳ和条件Ⅱ相比较,条件Ⅳ时可能增大了反应体系的压强 |
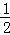 和
和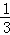 ;D的气态氢化物溶于水后显碱性.
;D的气态氢化物溶于水后显碱性.