用两根铂丝作电极插入KOH溶液中,再分别向两极通入甲烷气体和氧气,可形成燃料电池,该电池放电时的总反应为:CH4+2KOH+2O2═K2CO3+3H2O,下列说法错误的是( )
|
| A. | 通甲烷的一极为负极,通氧气的一极为正极 |
|
| B. | 放电时通入氧气的一极附近溶液的pH升高 |
|
| C. | 放电一段时间后,KOH的物质的量不发生变化 |
|
| D. | 通甲烷的电极反应式是:CH4+10OH﹣﹣8e﹣═CO32﹣+7H2O |
研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源.该电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电.关于该电池的下列说法不正确的是( )
|
| A. | 水既是氧化剂又是溶剂 |
|
| B. | 放电时正极上有氢气生成 |
|
| C. | 放电时OH﹣向正极移动 |
|
| D. | 总反应为:2Li+2H2O=2LiOH+H2↑ |
白磷与氧可发生如下反应:P4+5O2═P4O10.已知断裂下列化学键需要吸收的能量分别为:P﹣P:a kJ•mol﹣1、P﹣O:b kJ•mol﹣1、P=O:c kJ•mol﹣1、O=O:d kJ•mol﹣1.根据图示的分子结构和有关数据估算该反应的△H,其中正确的是( )
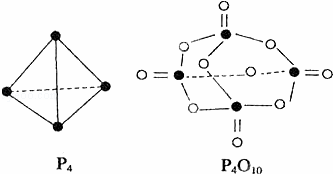
|
| A. | (6a+5d﹣4c﹣12b)kJ•mol﹣1 | B. | (4c+12b﹣6a﹣5d)kJ•mol﹣1 |
|
| C. | (4c+12b﹣4a﹣5d)kJ•mol﹣1 | D. | (4a+5d﹣4c﹣12b)kJ•mol﹣1 |
在﹣50℃时,液氨的电离跟水的电离相似,存在平衡,2NH3(l)⇌N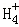 +N
+N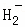 ,N
,N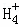 的平衡浓度为1×10﹣15mol•L﹣1,下列说法错误的是( )
的平衡浓度为1×10﹣15mol•L﹣1,下列说法错误的是( )
|
| A. | 在液氨中加入NaNH2,可使液氨的离子积变大 |
|
| B. | 在液氨中加入NH4Cl,液氨的离子积不变 |
|
| C. | 此温度下液氨的离子积K为1×10﹣30 |
|
| D. | 在液氨中加入金属钠可能有NaNH2生成 |
下列实验操作能达到目的是( )
|
| A. | 用Na2S溶液和Al2(SO4)3溶液反应制取Al2S3固体 |
|
| B. | 蒸干并灼烧AlCl3溶液可获得Al(OH)3固体 |
|
| C. | 用Na2S溶液和CuSO4溶液反应制取CuS固体 |
|
| D. | 蒸发MgCl2溶液制取MgCl2固体 |
分别取pH均等于2的盐酸和醋酸各l00mL,稀释2倍后,再分别加入足量锌粉,在相同条件下充分反应,下列有关叙述正确的是
( )
|
| A. | 反应开始时,盐酸和醋酸分别与锌反应的速率一样大 |
|
| B. | 反应开始时,盐酸与锌反应的速率大 |
|
| C. | 盐酸和醋酸分别与锌反应放出的氢气一样多 |
|
| D. | 醋酸与锌反应放出氢气多 |
下列说法正确的是( )
|
| A. | 在一定温度下的AgCl水溶液中,Ag+和Cl﹣浓度的乘积是一个常数 |
|
| B. | AgCl的Ksp=1.8×10﹣10 mol2•L﹣2,在任何含AgCl固体的溶液中,c(Ag+)=c(Cl﹣)且Ag+与Cl﹣浓度的乘积等于1.8×10﹣10 mol2•L﹣2 |
|
| C. | 温度一定时,当溶液中Ag+和Cl﹣浓度的乘积等于Ksp值时,此溶液为 AgCl的饱和溶液 |
|
| D. | 向饱和AgCl水溶液中加入少量盐酸,Ksp值变大 |
已知:Ksp(AgCl)=1.8×10﹣10,Ksp(AgI)=1.5×10﹣16,Ksp(Ag2CrO4)=2.0×10﹣12,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是( )
|
| A. | AgCl>AgI>Ag2CrO4 | B. | AgCl>Ag2CrO4>AgI |
|
| C. | Ag2CrO4>AgCl>AgI | D. | Ag2CrO4>AgI>AgCl |
相同物质的量浓度的NaCN和NaClO溶液相比,前者的pH较大,则下列有关同温、同体积和同浓度的HCN和HClO叙述中,正确的是( )
|
| A. | 酸性:HCN>HClO |
|
| B. | pH:HClO>HCN |
|
| C. | 浓度:c(CN﹣)<c(ClO﹣) |
|
| D. | 与NaOH恰好完全反应时,消耗NaOH的物质的量:HClO>HCN |
在BaSO3(s)⇌Ba2+(aq)+SO32﹣ (aq)平衡体系中,下列措施可使沉淀量减少的是( )
|
| A. | 加入K2SO3(s) | B. | 加入稀HNO3 | C. | 加入稀盐酸 | D. | 加入K2SO4(s) |