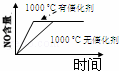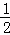COCl2(g)⇌CO(g)+Cl2(g);△H>0.当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是( )
|
| A. | ①②④ | B. | ①④⑥ | C. | ②③⑤ | D. | ③⑤⑥ |
已知X(g)+3Y(g)⇌2Z(g)的△H<0,在恒容密闭容器中反应达到平衡时,下列说法正确的是( )
|
| A. | 升高温度,平衡将正向移动 |
|
| B. | 3V正(X)═V逆(Y) |
|
| C. | 降低温度,混合气体的密度变小 |
|
| D. | 增加X的物质的量,Y的转化率降低 |
常温下,下列溶液中的微粒浓度关系正确的是( )
|
| A. | 新制氯水中加入固体NaOH:c(Na+)=c(Cl﹣)+c(ClO﹣)+c(OH﹣) |
|
| B. | pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3﹣)>c(CO32﹣)>c(H2CO3) |
|
| C. | pH=11的氨水与pH=3的盐酸等体积混合:c(Cl﹣)=c(NH4+)>c(OH﹣)=c(H+) |
|
| D. | 0.2mol/L的CH3COOH溶液与0.1mol/L的NaOH溶液等体积混合:2c(H+)﹣2c(OH﹣)=c(CH3COO﹣)﹣c(CH3COOH) |
25℃时将pH=3的强酸与pH=12的强碱溶液混合,所得溶液pH=10,则强酸与强碱的体积比是( )
|
| A. | 1:9 | B. | 9:1 | C. | 1:11 | D. | 11:9 |
T℃时,在2L的密闭容器中,A气体与B气体发生可逆反应生成C气体,反应过程中A、B、C物质的量变化如图(Ⅰ)所示.若保持其它条件不变,温度分别为T1和T2时,B的物质的量分数与时间关系如图(Ⅱ)所示.下列叙述正确的是( )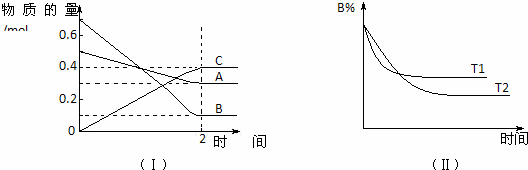
|
| A. | 2 min内A的化学反应速率为0.1 mol/(L•min) |
|
| B. | 在反应达平衡时,保持其他条件不变,增大压强,正逆反应速率都增大,且平衡向逆反应方向移动 |
|
| C. | 在反应达平衡时,其它条件不变,升高温度,正逆反应速率都增大,且A的转化率增大 |
|
| D. | 在T℃时,若A的浓度减少了1 mol/L,则B的浓度会减少3 mol/L,C的浓度会增加2 mol/L |
在4℃时下列溶液一定呈酸性的是( )
|
| A. | pH=7的溶液 |
|
| B. | 遇酚酞显无色的溶液 |
|
| C. | 含有H+的溶液 |
|
| D. | 溶液中由水电离出的C(OH﹣)=10﹣9 mol•L﹣1 |
在一定温度下,下列叙述不能作为可逆反应A(g)+3B(g)⇌2C(g)达到平衡的标志的是( )
①C的生成速率是B的生成速率的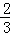 倍
倍
②单位时间生成a mol A,同时生成3a mol B
③A、B、C的浓度不再变化
④混合气体的总压强不再变化
⑤混合气体的物质的量不再变化
⑥单位时间消耗 a mol A,同时生成3a mol B
⑦A、B、C 的分子数目比为1:3:2.
|
| A. | ②⑦ | B. | ⑥④ | C. | ①③ | D. | ⑤⑥ |
可逆反应aA(s)+bB(g)⇋cC(g)+dD(g)△H=Q kJ•mol﹣1,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图所示,据图分析,以下正确的是( )
|
| A. | T1>T2,Q>0 | B. | T1<T2,Q<0 |
|
| C. | p1>p2,a+b=c+d | D. | p1<p2,a+b=c+d |
一定温度下,在体积为 VL 的密闭容器中加入1molX和1molY进行如下反应: X(g)+Y(g )═2Z(g )+W(s);△H>0达到平衡,下列判断正确的是( )
|
| A. | 向平衡混合物中加入少量W,正、逆反应速率均增大 |
|
| B. | 平衡后加入X,上述反应的△H增大 |
|
| C. | 温度不变,将容器的体积变为2VL,Z的平衡浓度变为原来的 |
|
| D. | 当容器中混合气体的压强不变时,可以证明此反应已达到平衡状态 |