在一密闭容器中加入A、B、C三种气体,保持温度一定,在t1~t4时刻测得各物质的浓度如表.据此判断下列结论正确的是( )
| 测定时刻/s | t1 | t2 | t3 | t4 |
| c(A)/(mol•L﹣1) | 6 | 3 | 2 | 2 |
| c(B)/(mol•L﹣1) | 5 | 3.5 | 3 | 3 |
| c(C)/(mol•L﹣1) | 1 | 2.5 | 3 | 3 |
|
| A. | 在t3时刻反应已经停止 |
|
| B. | A的转化率比B的转化率低 |
|
| C. | 该温度下此可逆反应平衡常数K=4 |
|
| D. | 该反应的化学方程式为2A(g)+B(g)⇌C(g) |
将1molSO2和1molO2通入一容积不变的密闭容器中,在一定温度和催化剂作用下发生反应 SO2(g)+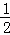 O2(g)⇌SO3(g).达到平衡后SO3为0.3mol,此时若移走0.5molSO2和0.5mol O2,则重新达到平衡后SO3物质的量为( )
O2(g)⇌SO3(g).达到平衡后SO3为0.3mol,此时若移走0.5molSO2和0.5mol O2,则重新达到平衡后SO3物质的量为( )
|
| A. | 等于0.3mol | B. | 等于0.15mol |
|
| C. | 小于0.15mol | D. | 大于0.15mol,小于0.3mol |
如图所示,隔板I固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:A(g)+2B(g)⇌xC(g)△H=﹣192kJ•mol﹣1,向M、N中都通入1mol A和2mol B的混合气体,初始M、N容积相同,保持温度不变.下列说法正确的是( )

|
| A. | 若x=3,达到平衡后A的体积分数关系为:φ(M)>φ(N) |
|
| B. | 若x>3,达到平衡后B的转化率关系为:α(M)>α(N) |
|
| C. | 若x<3,C的平衡浓度关系为:c(M)>c(N) |
|
| D. | x不论为何值,起始时向N容器中充入任意值的C,平衡后N容器中A的浓度均相等 |
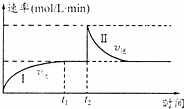
在一恒温体积可变的密闭容器中发生如下反应:A(g)+B(g)⇌2C(g)△H<0.t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图.下列说法正确的是( )
|
| A. | 0~t2时,v正>v逆 |
|
| B. | t2时刻改变的条件可能是加催化剂 |
|
| C. | Ⅰ、Ⅱ两过程达到反应限度时,A的体积分数Ⅰ=Ⅱ |
|
| D. | Ⅰ、Ⅱ两过程达到反应限度时,平衡常数I<Ⅱ |
A、B的混合气体在密闭容器中发生如下反应:xA(g)+yB(g)═zC(g)△H<0.达到化学平衡后测得A的浓度为0.5mol•L﹣1;保持温度不变,将密闭容器的容积缩小至原来的一半,再次达到平衡时,测得A的浓度为0.9mol•L﹣1.则下列有关判断正确的是( )
|
| A. | 平衡向正反应方向移动了 | B. | x+y<z |
|
| C. | B的转化率下降 | D. | C的体积分数减小 |
一定条件下,在一恒容密闭容器中,能表示反应 X(g)+2Y(g)⇌2Z(g) 一定达到化学平衡状态的是( )
①容器中气体的密度不再发生变化
②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成n mol Z,同时生成2n mol Y.
|
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
反应 H2(g)+I2(g)⇌2HI(g)的平衡常数K1;反应HI(g)⇌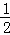 H2(g)+
H2(g)+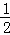 I2(g)的平衡常数K2,则K1、K2的关系为(平衡常数为同温度下的测定值)( )
I2(g)的平衡常数K2,则K1、K2的关系为(平衡常数为同温度下的测定值)( )
|
| A. | K1=2K2 | B. | K1=K22 | C. | K1= | D. | K1= |
下列说法正确的是( )
|
| A. | 在常温下,放热反应一般能自发进行,吸热反应都不能自发进行 |
|
| B. | NH4HCO3(s) |
|
| C. | 因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可单独作为反应自发性的判据 |
|
| D. | 在其他外界条件不变的情况下,使用催化剂可以改变化学反应进行的方向 |
下列事实不能用勒夏特利原理来解释的是( )
|
| A. | 用排饱和食盐水的方法收集氯气 |
|
| B. | 合成氨工业选择高温 |
|
| C. | 增大压强,有利于SO2和O2反应生成SO3 |
|
| D. | 在Fe3++3SCN ﹣⇌Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深 |
某浓度的氨水中存在下列平衡:NH3•H2O⇌NH4++OH﹣,如想增大NH4+的浓度,而不增大OH﹣的浓度,应采取的措施是( )
|
| A. | 适当升高温度 | B. | 加入NaOH固体 |
|
| C. | 通入NH3 | D. | 加入NH4Cl固体 |
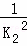
 K2
K2 NH3(g)+H2O(g)+CO2(g)△H=+185.57kJ/mol能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向
NH3(g)+H2O(g)+CO2(g)△H=+185.57kJ/mol能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向