“低碳循环”、如何降低大气中CO2的含量、有效地开发利用CO2,引起了全世界的普遍重视。
I. 用电弧法合成的储氢纳米碳管,可用如下氧化法提纯,请完成下述反应:
___  C+ ___ KMnO4 + 6 H2SO4→____CO
C+ ___ KMnO4 + 6 H2SO4→____CO 2↑+ ____MnSO4 + ____K2SO4 + 6 H2
2↑+ ____MnSO4 + ____K2SO4 + 6 H2 O
O
II.某研究小组现将三组CO(g)与H2O(g)的混合气体分别通入体积为2 L的恒容密闭容器中,一定条件下发生反应:CO(g)+H2O(g) CO2(g)+H2(g) △H<0,得到如下数据:
CO2(g)+H2(g) △H<0,得到如下数据:
| 实验组 | 温度/℃ | 起始量(mol) | 平衡量(mol) | 达到平衡所 需要时间/min | ||
| CO(g) | H2O(g) | CO2(g) | H2(g) | |||
| I | 800 | 2 | 2 | x | 1 | 5 |
| II | 900 | 1 | 2 | 0.5 | 0.5 | tm |
| III | 900 | 2 | 4 | y | y | tn |
(1)实验I中,前5min的反应速率υ(CO2)= mol•L1•min1。
(2)下列能判断在800℃实验条件下CO(g)与H2O(g)反应一定达到平衡状态的是 。
A.容器内压强不再变化 B.
 C.混合气体密度不变 D.υ正(CO) =
C.混合气体密度不变 D.υ正(CO) = υ逆(CO2)
υ逆(CO2)
(3)实验III中:y= 。
(4)若实验Ⅲ的容器改为在绝热的密闭容器中进行,实验
测得H2O(g)的转化率a(H2O)随时间变化的示意图,
如右图 所示,b点:υ正 υ逆(填“<”.“=”或“>”)。
所示,b点:υ正 υ逆(填“<”.“=”或“>”)。

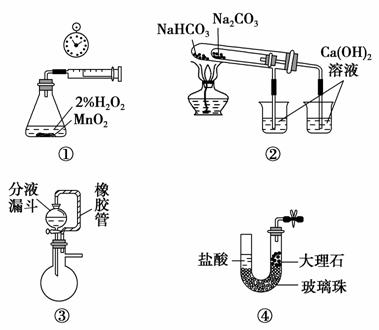
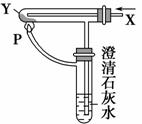
 用如图所示装置进行下列实验,能达到实验目的的是 ( )。
用如图所示装置进行下列实验,能达到实验目的的是 ( )。
 实验步骤:
实验步骤:
 代反应的有 (填序号)。
代反应的有 (填序号)。 与碳酸氢钠反应的G的同分异构体共有
与碳酸氢钠反应的G的同分异构体共有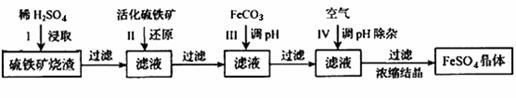
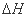 = —1648kJ/mol
= —1648kJ/mol
 。
。
 2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中物质的物质的量浓度.反应速率分别随时间的变化如下图所示:
2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中物质的物质的量浓度.反应速率分别随时间的变化如下图所示: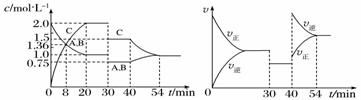
 ,聚乳酸是由单体之间通过加聚而合成
,聚乳酸是由单体之间通过加聚而合成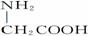 )和丙氨酸(
)和丙氨酸( )缩合最多可形成4种二肽
)缩合最多可形成4种二肽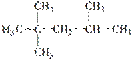 的系统命名法的名称为2,2,3-三甲基戊烷
的系统命名法的名称为2,2,3-三甲基戊烷