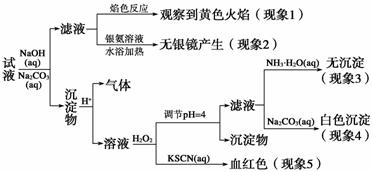
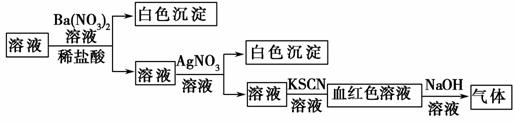
已知某溶液X可能由K+、Mg2+、Cu2+、Ag+、Ba2+、Al3+、Fe2+、AlO 、CO
、CO 、SO
、SO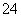 、I-、SiO
、I-、SiO 、MnO
、MnO 中的若干种离子组成。某化学兴趣小组通过下列实验确定了其组成。
中的若干种离子组成。某化学兴趣小组通过下列实验确定了其组成。
(1)根据下列实验步骤和现象,推断实验结论:
| 实验步骤与实验现象 | 实验结论 |
| Ⅰ.观察溶液:无色透明 | ①原溶液中一定不含的离子是____________ |
| Ⅱ.取适量该溶液,加入过量的硝酸,有气体生成,并得到无色溶液 | ②原溶液中一定不含的离子是__________________________,一定含有的离子是________ |
| Ⅲ.在Ⅱ所得溶液中再加入过量的碳酸氢铵溶液,有气体生成,同时析出白色沉淀A | ③原溶液中还一定含有的离子是________,生成沉淀A的离子方程式为___________________ |
| Ⅳ.在Ⅲ所得溶液中再逐滴加入氢氧化钡溶液至过量,加热也有气体生成,同时析出白色沉淀B | ④白色沉淀B中一定含有_____ __,可能含有________________ |
(2)上述实验步骤Ⅳ中开始阶段发生反应的离子方程式一定有____________。

(3)该化学兴趣小组的同学为了进一步确定B的成分,取一定量经洗涤后的B与Y溶液反应,白色固体的物质的量与Y溶液体积之间的关系如图所示。
Y可能为______________________。B的组成为_______________________。
(4)已知氢氧化铝电离出H+比碳酸氢钠电离出H+更难。根据上述推断,取少量原溶液于试管中,向试管中滴加少量硫酸氢钠稀溶液至过量,按先后顺序可以观察到的现象有_____________________________________________。
写出最后发生反应的离子方程式:____________________________________。
向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是
( )。
| 操作 | 现象 | 结论 | |
| A | 滴加BaCl2溶液 | 生成白色沉淀 | 原溶液中有SO |
| B | 滴加氯水和CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
| C | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+,无K+ |
| D | 滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH |
下列对各组离子或物质是否能够大量共存解释正确的是
( )。
| A | 常温常压下NH3、O2、H2、CO2 | 不能共存 | NH3为碱性气体、CO2为酸性气体,二者反应生成(NH4)2CO3 |
| B | c(OH-)=1.0×10-13 mol·L-1溶液中,Fe2+、NO | 不能共存 | 发生反应:3Fe2++NO |
| C | 溶液中:K+、Cu2+、Cl-、NH3·H2O | 不能共存 | 发生反应:Cu2++2OH-===Cu(OH)2↓ |
| D | 溶液中:Al3+、Na+、SO | 可以共存 | 不能发生反应 |
 中的若干种。某研究性学习小组为探究溶液X的组成,进行如下实验(其中Y为无色无味的气体):
中的若干种。某研究性学习小组为探究溶液X的组成,进行如下实验(其中Y为无色无味的气体):