(1)用分液漏斗、锥形瓶、导管、注射器、双孔胶塞、秒表和铁架台 (选填“可以”、“不可以”)测定锌和稀硫酸反应生成氢气的反应速率
(2)为证明盐的水解是吸热反应,四位学生分别设计了如下实验方案,其中正确的是___
甲.在醋酸钠溶液中滴入2滴酚酞,加热后红色加深,说明盐类水解是吸热反应
乙.用等浓度纯碱溶液去油污,热溶液比冷溶液效果好,说明盐类水解是吸热反应
丙.将硝酸铵晶体溶于水,水温下降,说明盐类水解是吸热反应
丁.在氨水中加入氯化铵固体,溶液的pH变小,说明盐类水解是吸热反应
(3)用标准NaOH溶液滴定未知浓度的盐酸溶液,下列操作造成测定结果偏高的是
A.酸式滴定管用蒸馏水洗净后,未用待测盐酸润洗
B.滴定前,碱式滴定管尖嘴有气泡,滴定后气泡消失
C.滴定终点读数时,仰视滴定管刻度,其他操作正确
(4)用物质的量浓度为0.1000 mol/L的KMnO4(H+)溶液滴定未知浓度的H2C2O4(弱酸)溶液,分别取20.00 mL 草酸溶液于3个洁净的锥形瓶中,用标准的KMnO4(H+)溶液滴定至终点,数据如下:
| 测定次数 | 第一次 | 第二次 | 第三次 |
| 初始读数(mL) | 0.40 | 0.90 | 0.00 |
| 终点读数(mL) | 25.05 | 21.00 | 19.90 |
已知:相关反应方程式为:5H2C2O4+2KMnO4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
请回答下列问题:
① 标准KMnO4溶液应装在 (选填“酸式”或“碱式”)滴定管中;
② 判断已达滴定终点的现象是:____________________________________ ;
③ 实验测得草酸溶液的物质的量浓度为_____________mol/L。(保留四位有效数字)
合成氨是人类科学技术上的一项重大突破,其反应原理为
N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1。
2NH3(g) ΔH=-92.4 kJ·mol-1。
(1) T℃时在2L的密闭容器中,N2、H2混合气体充分反应5min后放出热量46.2 kJ,
用H2表示的平均速率为 。
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
(2)合成氨厂可用反应CO(g)+H2O(g) H2(g)+CO2(g)获得H2,已知该反应的平衡
H2(g)+CO2(g)获得H2,已知该反应的平衡
常数随温度的变化如右表,试回答下列问题:
① 在800℃发生上述反应,向恒容反应器投入CO2、H2 、CO、 H2O的物质的量分别为:1 mol 、1 mol 、2 mol 、2 mol,此时该反应由 反应方向开始建立平衡。
(选填“正”或“逆”)。
② 在500℃时进行上述反应,若CO、H2O的起始浓度均为0.020 mol·L-1 ,在该条件下,CO的最大转化率为 。
③ 在其他条件不变的前提下,下列措施一定可以提高H2的百分含量的有___________;
a.增加CO的用量 b.增加H2O(g)的用量
c.增大压强 d.降低温度
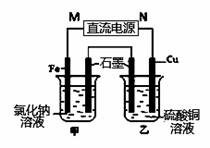 (3)如右图装置中甲烧杯盛放100 mL 0.2 mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5 mol/L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红,乙烧杯中石墨电极附近pH值的变化为 (选填“变大”、“变小”、“不变”)。通电一段时间后(溶液中还有CuSO4),若要使乙烧杯中电解质溶液恢复到电解前的状态,可加入 (填序号).
(3)如右图装置中甲烧杯盛放100 mL 0.2 mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5 mol/L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红,乙烧杯中石墨电极附近pH值的变化为 (选填“变大”、“变小”、“不变”)。通电一段时间后(溶液中还有CuSO4),若要使乙烧杯中电解质溶液恢复到电解前的状态,可加入 (填序号).