0 144561 144569 144575 144579 144585 144587 144591 144597 144599 144605 144611 144615 144617 144621 144627 144629 144635 144639 144641 144645 144647 144651 144653 144655 144656 144657 144659 144660 144661 144663 144665 144669 144671 144675 144677 144681 144687 144689 144695 144699 144701 144705 144711 144717 144719 144725 144729 144731 144737 144741 144747 144755 203614
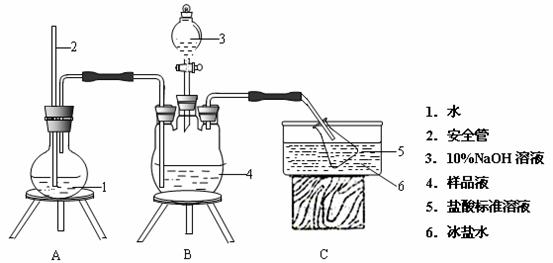
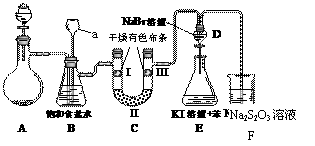

 (1)上图中设计装置D、E的目的是比较氯、溴、碘的非金属性,有同学认为该设计不能达到实验目的,其理由是 。该组的同学思考后将上述D、E、F装置改为实验操作步骤如下:
(1)上图中设计装置D、E的目的是比较氯、溴、碘的非金属性,有同学认为该设计不能达到实验目的,其理由是 。该组的同学思考后将上述D、E、F装置改为实验操作步骤如下: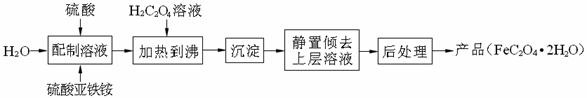
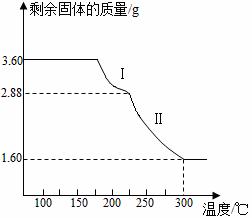
 CH3OH(g)+H2O(g) ΔH
CH3OH(g)+H2O(g) ΔH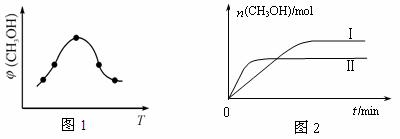
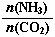 =3进行反应,达平衡时CO2的转化率为60%,则NH3的平衡转化率为 。
=3进行反应,达平衡时CO2的转化率为60%,则NH3的平衡转化率为 。 SO2(g) + Cl2(g) K1 △H=a kJ/mol (Ⅰ)
SO2(g) + Cl2(g) K1 △H=a kJ/mol (Ⅰ)