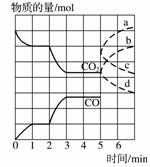
在100℃时,将N2O4、NO2分别充入两个各为1 L的密闭容器中,反应过程中浓度变化如下:[2NO2(g)  N2O4(g) ΔH<0]
N2O4(g) ΔH<0]
| 容器 | 物质 | 起始浓度/(mol·L-1) | 平衡浓度/(mol·L-1) |
| Ⅰ | N2O4 | 0.100 | 0.040 |
| NO2 | 0 | 0.120 | |
| Ⅱ | N2O4 | 0 | 0.014 |
| NO2 | 0.100 | 0.072 |
下列说法正确的是
A. 平衡时,Ⅰ、Ⅱ中反应物的转化率α(N2O4)<α(NO2)
B. 平衡时,Ⅰ、Ⅱ中上述正反应的平衡常数K(Ⅰ) = 2K(Ⅱ)
C. 平衡后,升高相同温度,以N2O4表示的反应速率ν(Ⅰ)<ν(Ⅱ)
D. 平衡后,升高温度,Ⅰ、Ⅱ中气体颜色都将变深
下列说法正确的是
A.HClO2 →ClO2+Cl2+H2O(未配平), 1 mol HClO2分解时转移电子的物质的量为1 mol
B.标准状况下,14 g CO、C2H4混合气体与11.2 L N2所含有的分子数都是0.5NA
C.与金属Cu常温下反应放出气体的溶液可以存在的离子有:Fe2+、Al3+、SO42-、K+
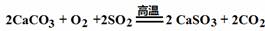
| |
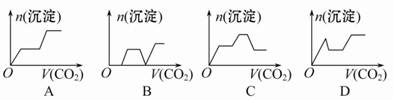
当身处贴有下列标志的环境时,行为不正确的是
| A | B | C | D | |||||
| 环境 |
|
|

 |
| ||||
| 行为 | 切勿随意进入 | 严禁烟火 | 尽量远离 | 顺风向低处跑 |
已知反应:2CH3OH(g)CH3OCH3(g)+H2O(g)。某温度下的平衡常数为400。在此温度下,向密闭容器中加入一定量CH3OH,反应到5 min时测得各组分的浓度如表所示:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/mol·L-1 | 0.44 | 0.6 | 0.6 |
(1)该反应在低温下(此时水为液态)能自发进行,则该反应的ΔH______0(填“>”、“<”或“=”,下同)。
(2)比较此时正、逆反应速率的大小:v正______v逆。
(3)前5 min时,用CH3OCH3表示该反应的速率为________________。
(4)再过一段时间后,反应达到平衡状态。能判断该反应已达到化学平衡状态的依据是__________(填字母)。
A.容器中压强不变
B.混合气体中c(CH3OH)不变
C.v生成(CH3OH)=2v消耗(H2O)
D.c(CH3OCH3)=c(H2O)
(5)达到平衡状态时,CH3OH的转化率为__________。
一定条件下,体积为1 L的密闭容器中发生如下反应:
SiF4(g)+2H2O(g)SiO2(s)+4HF(g)
ΔH=148.9 kJ·mol-1。
(1)下列各项中能说明该反应已达化学平衡状态的是__________(填字母)。
a.v消耗(SiF4)=4v生成(HF)
b.容器内气体压强不再变化
c.容器内气体的总质量不再变化
d.HF的体积分数不再变化
(2)反应过程中测定的部分数据如下表(表中t2>t1)所示。
| 反应时间/min | n(SiF4)/mol | n(H2O)/mol |
| 0 | 1.20 | 2.40 |
| t1 | 0.80 | a |
| t2 | b | 1.60 |
通过a或b的值及化学平衡原理说明t1时反应是否达到化学平衡状态:__________。
(3)若只改变一个条件使上述反应的化学平衡常数变大,该反应________(填字母)。
a.一定向正反应方向移动
b.一定向逆反应方向移动
c.一定是减小压强造成的
d.一定是升高温度造成的
e.SiF4的平衡转化率一定增大
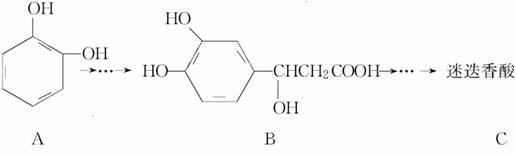
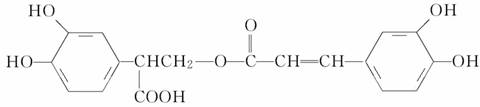 ,以邻苯二酚为原料合成迷迭香酸的路线为
,以邻苯二酚为原料合成迷迭香酸的路线为