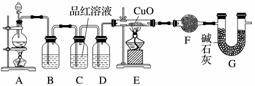
(1)已知Na2S2O3+H2SO4===Na2SO4+S↓+SO2↑+H2O。甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。设计实验如下(所取溶液体积均为10 mL):
| 实验编号 | 实验温度/℃ | c(Na2S2O3)/mol·L-1 | c(H2SO4)/mol·L-1 |
| ① | 25 | 0.1 | 0.1 |
| ② | 25 | 0.2 | 0.1 |
| ③ | 25 | 0.1 | 0.2 |
| ④ | 50 | 0.2 | 0.1 |
| ⑤ | 50 | 0.1 | 0.1 |
其他条件不变时,探究温度对化学反应速率的影响,应选择__________(填实验编号);探究浓度对化学反应速率的影响,应选择__________(填实验编号);若同时选择①②③溶液测定变浑浊的时间,是探究__________对化学反应速率的影响。
(2)已知Na2S2O3溶液与Cl2反应时,1 mol Na2S2O3转移 8 mol 电子,该反应的离子方程式是________________________________________________________________________。
甲同学设计如下实验流程探究Na2S2O3的化学性质。
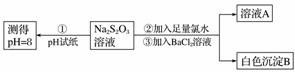
(Ⅰ)甲同学设计实验流程的目的是证明Na2S2O3溶液具有碱性和________性。
(Ⅱ)加入BaCl2溶液生成白色沉淀B的离子方程式是
________________________________________________________________________。
(Ⅲ)乙同学认为应将上述流程中②③所加试剂顺序颠倒,你认为甲、乙两同学的设计更合理的是________(填“甲”或“乙”),理由是_____________________________。
某合作小组同学将铜片加入稀硝酸中,发现开始时反应非常慢,一段时间后反应速率明显加快。该小组通过实验探究其原因。
(1)该反应的离子方程式为______________________________________。
(2)提出合理假设,该实验中反应速率明显加快的原因可能是______(填字母)。
A.反应放热导致温度升高
B.压强增大
C.生成物的催化作用
D.反应物接触面积增大
(3)初步探究,测定反应过程中不同时间溶液的温度,结果如表所示:
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 35 | 50 | 60 | 70 | 80 |
| 温度/℃ | 25 | 26 | 26 | 26 | 26 | 26 | 26.5 | 27 | 27 | 27 | 27 |
结合实验目的和表中数据,你得出的结论是__________________________。
(4)进一步探究:查阅文献了解到化学反应的产物(含中间产物)可能对反应有催化作用。请完成以下实验设计表并将实验目的补充完整:
| 实验编号 | 铜片质量/g | 0.1 mol·L-1的硝酸体积/mL | 硝酸铜晶体/g | 亚硝酸钠晶体/g | 实验目的 |
| ① | 5 | 20 | 实验①和②探究____的影响;实验①和③探究NO | ||
| ② | 0.5 | ||||
| ③ | 0.5 |
某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有___________________________。
(2)硫酸铜溶液可以加快氢气生成速率的原因是______________________。
(3)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与上述实验中CuSO4溶液起相似作用的是________。
(4)要加快上述实验中气体产生的速率,还可采取的措施有______(答两种)。
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列的实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
| 实验 混合溶液 | A | B | C | D | E | F |
| 4 mol·L-1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
①请完成此实验设计,其中:V1=__________________,V6=__________,V9=________;
②反应一段时间后,实验A中的金属呈________色,实验E中的金属呈________色;
③该同学最后得出的结论为当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:________________________________________________________________________
________________________________________________________________________。
某化学兴趣小组的同学学习了同周期元素性质递变规律后,设计了一套实验方案进行实验探究,并记录了有关实验现象如下表:
| 实验操作 | 实验现象 |
| Ⅰ.用砂纸打磨后的镁带与沸水反应,再向反应后溶液中滴加酚酞 | A.浮于水面,熔成一个小球,在水面上无定向移动,随之消失,溶液变红色 B.产生气体,可在空气中燃烧,溶液变成浅红色 C.反应不十分强烈,产生的气体可以在空气中燃烧 D.剧烈反应,产生可燃性气体 E.生成白色胶状沉淀,进而沉淀消失 F.生成淡黄色沉淀 |
| Ⅱ.向新制的H2S饱和溶液中滴加新制的氯水 | |
| Ⅲ.钠与滴有酚酞溶液的冷水反应 | |
| Ⅳ.镁带与2 mol·L-1的盐酸反应 | |
| Ⅴ.铝条与2 mol·L-1的盐酸反应 | |
| Ⅵ.向AlCl3溶液滴加NaOH溶液至过量 |
请你帮助该同学整理并完成实验报告
(1)实验目的:_____________________________________。
(2)实验用品:仪器①______________、②____________、③____________、④试管夹、⑤镊子、⑥小刀、⑦玻璃片、⑧砂纸、⑨胶头滴管等。
药品:钠、镁带、铝条、2 mol·L-1的盐酸、新制的氯水、新制的饱和H2S溶液、AlCl3溶液、NaOH溶液等。
(3)请你写出上述的实验操作与对应的现象
Ⅰ________、Ⅱ________、Ⅲ________、Ⅳ________、Ⅴ________、Ⅵ________。(用A~F表示)
写出实验操作Ⅱ、Ⅵ的离子反应方程式
实验Ⅱ________________________________________________________________________;
实验Ⅵ________________________________________________________________________。
(4)实验结论:_________________________。
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法探究影响化学反应速率的因素。
实验一:利用Cu、Fe、Mg和不同浓度的硫酸(0.5 mol·L-1、2 mol·L-1、18.4 mol·L-1),设计实验方案,研究影响反应速率的因素。
(1)甲同学的实验报告如表所示:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取三份等体积的2 mol·L-1硫酸于试管中 ②分别投入大小、形状相同的Cu、Fe、Mg | 反应产生气泡的速率大小:Mg>Fe>Cu | 反应物的性质越活泼,反应速率越大 |
该同学的实验目的是__________________,要想得出正确的实验结论,还需要控制的实验条件是________________________________________________________________________。
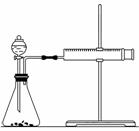
(2)乙同学为了能精确地研究浓度对反应速率的影响,在相同温度下利用如图所示装置进行定量实验。完成该实验应选用的实验药品是__________,应该测定的实验数据是____________。
实验二:已知2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+8H2O+10CO2↑,在开始一段时间内反应速率较小,溶液褪色不明显,但反应一段时间后,溶液突然褪色,反应速率明显增大。
(3)针对上述实验现象,某同学认为该反应放热,导致溶液的温度升高,从而使反应速率增大。从影响化学反应速率的因素看,你认为还可能是________的影响。
(4)若要用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,还可以在反应开始时加入________(填字母)。
A.硫酸钾 B.硫酸锰
C.氯化锰 D.水
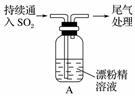
某学生对SO2与漂粉精的反应进行实验探究:
| 操 作 | 现 象 |
| 取4 g漂粉精固体,加入100 mL水 | 部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的pH | pH试纸先变蓝(约为12),后褪色 |
|
| ⅰ.液面上方出现白雾; ⅱ.稍后,出现浑浊,溶液变为黄绿色; ⅲ.稍后,产生大量白色沉淀,黄绿色褪去 |
(1)Cl2和Ca(OH)2制取漂粉精的化学方程式是___________________________。
(2)pH试纸颜色的变化说明漂粉精溶液具有的性质是________。
(3)向水中持续通入SO2,未观察到白雾。推测现象ⅰ的白雾由HCl小液滴形成,进行如下实验:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用酸化的AgNO3溶液检验白雾,产生白色沉淀。
①实验a的目的是________。
②由实验a、b不能判断白雾中含有HCl,理由是____________________________。
(4)现象ⅱ中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的有效成分和Cl-发生反应。通过进一步实验确认了这种可能性,其实验方案是________。
(5)将A瓶中混合物过滤、洗涤,得到沉淀X。
①向沉淀X中加入稀HCl,无明显变化。取上层清液,加入BaCl2溶液,产生白色沉淀。则沉淀X中含有的物质是________。
②用离子方程式解释现象ⅲ中黄绿色褪去的原因:_____________________________。
 的影响
的影响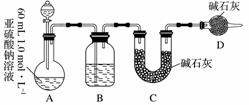
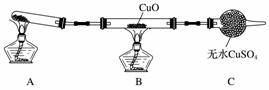
 ZnSO4+SO2↑+2H2O计算后,取65.0 g锌粒与98%的浓H2SO4(ρ=1.84 g·cm-3)110 mL充分反应,锌全部溶解,对于制得的气体,有同学认为可能混有杂质。
ZnSO4+SO2↑+2H2O计算后,取65.0 g锌粒与98%的浓H2SO4(ρ=1.84 g·cm-3)110 mL充分反应,锌全部溶解,对于制得的气体,有同学认为可能混有杂质。