镁、铜等金属离子是人体内多种酶的辅因子。工业上从海水中提取镁时,先制备无水氯化镁,然后将其熔融电解,得到金属镁。
(1)以MgCl2为原料用熔融盐电解法制备镁时,常加入NaCl、KCl或CaCl2等金属氯化物,其主要作用除了降低熔点之外还有____________________________________________。
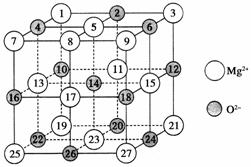
(2)已知MgO的晶体结构属于NaCl型。某同学画出的MgO晶胞结构示意图如上图所示,请改正图中错误:________________。
(3)Mg是第3周期元素,该周期部分元素氟化物的熔点见下表:
| 氟化物 | NaF | MgF2 | SiF4 |
| 熔点/K | 1 266 | 1 534 | 183 |
解释表中氟化物熔点差异的原因:________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
已知:硅酸盐和石英的晶格能如下表:
| 硅酸盐矿物和石英 | 晶格能(kJ·mol-1) |
| 橄榄石 | 4 400 |
| 辉石 | 4 100 |
| 角闪石 | 3 800 |
| 云母 | 3 800 |
| 长石 | 2 400 |
| 石英 | 2 600 |
回答下列问题:
(1)橄榄石和云母晶出的顺序是______________。
(2)石英总是在各种硅酸盐析出后才晶出的原因是__________。
(3)推测云母和橄榄石的熔点顺序为______________________,硬度大小为_______。
参考表中物质的熔点,回答有关问题。
| 物质 | NaF | NaCl | NaBr | NaI | NaCl | KCl | RbCl | CsCl |
| 熔点/℃ | 995 | 801 | 755 | 651 | 801 | 776 | 715 | 646 |
| 物质 | SiF4 | SiCl4 | SiBr4 | SiI4 | SiCl4 | GeCl4 | SnCl4 | PbCl4 |
| 熔点/℃ | -90.2 | -70.4 | 5.2 | 120.0 | -70.4 | -49.5 | -36.2 | -15.0 |
(1)钠的卤化物及碱金属的氯化物的熔点与卤离子及碱金属离子的__________有关,随着__________的增大,熔点依次降低。
(2)硅的卤化物及硅、锗、锡、铅的氯化物的熔点与________________有关,随着________________增大,________________增大,故熔点依次升高。
(3)钠的卤化物的熔点比相应的硅的卤化物的熔点高得多,这与__________有关,因为一般__________比__________的熔点高。
有下列离子晶体空间示意图:(·阳离子,∘阴离子):
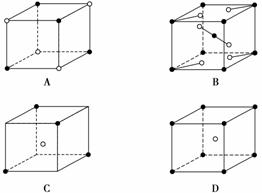
以M代表阳离子,以N表示阴离子,写出各离子晶体的组成表达式:A__________、B__________、C________、D________。