常温下,下列溶液的pH或微粒的物质的量浓度关系正确的是( )
|
| A. | Ca(ClO)2溶液中:c(Ca2+)>c(ClO﹣)>c(OH﹣)>c(H﹣) |
|
| B. | 等体积、等物质的量浓度的Na2SO3溶液与NaHSO3溶液混合:c(Na+)=c(SO32﹣)+c(HSO3﹣)+c(H2SO3) |
|
| C. | 将0.2mol.L﹣1的某一元酸HA溶液和0.1mol.L﹣1的NaOH溶液等体积混合后溶液的pH大于7,则反应后的混合液:2c(OH﹣)+c(A﹣)=2c(H+)+c(HA) |
|
| D. | 某溶液中水电离出的c(OH﹣)=1×10﹣amol.L﹣1若a>7时,则pH该溶液的一定为14﹣a |
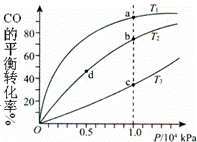
用CO和H2合成CH3OH的化学方程式为CO(g)+2H2(g)═CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是( )
|
| A. | 温度:T1>T2>T3 |
|
| B. | 正反应速率:υ(a)>υ(c) υ(b)>υ(d) |
|
| C. | 平衡常数:K(a)>K(c) K(b)=K(d) |
|
| D. | 平均摩尔质量:M(a)<M(c) M(b)<M(d) |
下列关于甲、乙、丙、丁四个图象的说法中,正确的是( )
|
| A. |
是等质量的两份锌粉a、b分别加到过量的稀硫酸中,同时向a中加入少量CH3COONa溶液,产生H2的体积V(L)与时间t(min)的关系图 |
|
| B. |
足量CO2不断通入含KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀与通入CO2的体积的关系图 |
|
| C. |
由图可知,双氧水在有催化剂存在时的热化学方程式为:2H2O2(l)=2H2O(l)+O2(g)△H=﹣2(Ea2′﹣Ea2) kJ•mol﹣1 |
|
| D. |
装置图能实现铁上镀锌 |
已知常温下,浓度均为0.1mol•L﹣1的4种钠盐溶液pH如下表:下列说法中正确的是( )
| 溶质 | Na2CO3 | NaClO | NaHCO3 | NaHSO3 |
| pH | 11.6 | 10.3 | 8.3 | 5.2 |
|
| A. | 足量SO2通入NaClO溶液中发生反应的离子方程式为:H2O+SO2+ClO﹣=HClO+HSO3﹣ |
|
| B. | 向氯水中加入NaHCO3,可以增大氯水中次氯酸的浓度 |
|
| C. | 常温下,相同物质的量浓度的H2SO3、H2CO3、HClO溶液,pH最大的是H2SO3 |
|
| D. | NaHSO3溶液中离子浓度大小顺序为:c(Na+)>c(H+)>c(HSO3﹣)>c(SO32﹣)>c(OH﹣) |
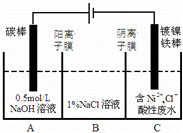
工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示.下列说法不正确的是( )已知:①Ni2+在弱酸性溶液中发生水解 ②氧化性:
Ni2+(高浓度)>H+>Ni2+(低浓度)
|
| A. | 碳棒上发生的电极反应:4OH﹣﹣4e﹣═O2↑+2H2O |
|
| B. | 电解过程中,B中NaCl溶液的物质的量浓度将不断减少 |
|
| C. | 为了提高Ni的产率,电解过程中需要控制废水pH |
|
| D. | 若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变 |
下列有关生活生产中的叙述合理的是( )
|
| A. | 硫酸工业中SO2转化为SO3时采用常压,是因为增大压强不会提高SO2的转化率 |
|
| B. | 打开啤酒瓶的瓶盖,有大量的气泡冒出来,该现象不能用勒夏特列原理解释 |
|
| C. | 氯碱工业中用离子交换膜电解槽电解时,往阴极室注入经过精制的饱和NaCl溶液,往阳极室注入稀氢氧化钠溶液(或去离子水) |
|
| D. | 工业上合成氨采用500℃左右的温度,最主要原因是该反应的催化剂在500℃左右时活性最好 |
下列说法不正确的是( )
|
| A. | 金属汞洒落,必须尽可能收集起来,并将硫磺粉撒在洒落的地方,使金属汞转变成不挥发的硫化汞 |
|
| B. | 滴定管在使用前要用待装液润洗,而容量瓶不用润洗 |
|
| C. | AlCl3溶液蒸干、灼烧至恒重,最终剩余固体是AlCl3 |
|
| D. | 碘单质与食盐的分离常用升华法,而碘水中提取碘单质则常用萃取法 |