25℃和1.01×105Pa时,反应2N2O5(g)=4NO2(g)+O2(g)△H=+56.76kJ/mol,自发进行的原因是( )
|
| A. | 是吸热反应 | B. | 是放热反应 |
|
| C. | 是熵减少的反应 | D. | 熵增大效应大于能量效应 |
下列措施肯定能使化学反应速率增大的是( )
|
| A. | 增大反应物的量 | B. | 增加压强 |
|
| C. | 升高温度 | D. | 使用催化剂 |
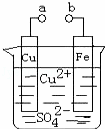
某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )
|
| A. | a和b不连接时,铁片上会有金属铜析出 |
|
| B. | a和b用导线连接时,铜片上发生的反应为:Cu2++2e﹣=Cu |
|
| C. | 无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 |
|
| D. | a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动 |
以KCl和ZnCl2混合液为电镀液在铁制品上镀锌,下列说法正确的是( )
|
| A. | 未通电前上述镀锌装置可构成原电池,电镀过程是该原电池的充电过程 |
|
| B. | 因部分电能转化为热能,电镀时通过的电量与锌的析出量无确定关系 |
|
| C. | 铁制品应该连接在直流电源的负极 |
|
| D. | 镀锌层破损后即对铁制品失去保护作用 |
(1)已知胆矾失水的化学反应方程式为:CuSO4•5H2O(s)=CuSO4(s)+5H2O(l);△H=+Q1kJ/mol
(2)室温下,无水硫酸铜溶于水的热化学方程式为:
CuSO4(s)=Cu2+(aq)+SO42﹣(aq);△H=﹣Q2kJ/mol
(3)胆矾溶于水时,溶液温度降低.Q1与Q2的关系是(Q1、Q2为正数)( )
|
| A. | Q1>Q2 | B. | Q1=Q2 | C. | Q1<Q2 | D. | 无法确定 |
2008年10月8日,美籍华裔科学家钱永健获得2008年度诺贝尔化学奖.16岁时,他凭借一个金属易受硫氰酸盐腐蚀的调查项目,荣获“美国西屋科学天才奖”.下列叙述正确的是( )
|
| A. | 金属腐蚀就是金属失去电子被还原的过程 |
|
| B. | 将水库中的水闸(钢板)与外加直流电源的负极相连,正极连接到一块废铁上可防止水闸被腐蚀 |
|
| C. | 合金的熔点都高于它的成分金属,合金的耐腐蚀性也都比其成分金属强 |
|
| D. | 铜板上的铁铆钉处在潮湿的空气中直接发生反应:Fe﹣3e﹣=Fe3+,继而形成铁锈 |
下列关于热化学反应的描述中正确的是( )
|
| A. | HCl和NaOH反应的中和热△H=﹣57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(﹣57.3)kJ/mol |
|
| B. | CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)═2CO(g)+O2(g)反应的△H=+566.0kJ/mol |
|
| C. | 需要加热才能发生的反应一定是吸热反应 |
|
| D. | 1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
在体积可变的容器中发生反应N2+3H2⇌NH3当增大压强使容器体积缩小时,化学反应速率加快,其主要原因是( )
|
| A. | 分子运动速率加快,使反应物分子间的碰撞机会增多 |
|
| B. | 反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多 |
|
| C. | 活化分子百分数未变,但单位体积内活化分子数增加,有效碰撞次数增多 |
|
| D. | 分子间距离减小,使所有的活化分子间的碰撞都成为有效碰撞 |
|
| D. | 分子间距离减小,使所有的活化分子间的碰撞都成为有效碰撞 |
有a、b、c、d四种金属,将a与b用导线连接起来,浸入电解质溶液中,b不易腐蚀;将a、d分别投入等浓度盐酸中,d比a反应激烈;将铜浸入b的盐溶液中,无明显变化;若将铜浸入c的盐溶液中,有金属c析出,据此判断它们的活动性由强到弱的顺序是( )
|
| A. | d>c>a>b | B. | d>a>b>c | C. | d>b>a>c | D. | b>a>d>c |