下面是四种盐在不同温度下的溶解度(g/100g水)
| NaNO3 | KNO3 | NaCl | KCl | |
| 10℃ | 80.5 | 20.9 | 35.7 | 31.0 |
| 100℃ | 175 | 246 | 39.1 | 56.6 |
(计算时假定:①盐类共存时不影响各自的溶解度;②过滤晶体时,溶剂损耗忽略不计)
取23.4 g NaCl和40.4 g KNO3,加70.0 g H2O,加热溶解,在100℃时蒸发掉50.0 g H2O,维持该温度,过滤析出晶体。计算所得晶体的质量(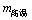 );将滤液冷却到10℃,待充分结晶后、过滤,计算所得晶体的质量(
);将滤液冷却到10℃,待充分结晶后、过滤,计算所得晶体的质量(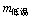 )。
)。
下表是四种盐的溶解度(g)。
|
| 0 | 10 | 20 | 30 | 40 | 60 | 80 | 100 |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.3 | 38.4 | 39.8 |
| NaNO3 | 73 | 80 | 88 | 96 | 104 | 124 | 148 | 180 |
| KCl | 27.6 | 31 | 34.0 | 37.0 | 40.0 | 45.5 | 51.1 | 56.7 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 110.0 | 169 | 246 |
请设计一个从硝酸钠和氯化钾制备纯硝酸钾晶体的实验(要求写出化学方程式及实验步骤)。
已知CO2过量时,CO2与NaOH反应生成NaHCO3(CO2+NaOH=NaHCO3)。参照物质的溶解度,用NaOH(固)、CaCO3(固)、水、盐酸为原料制取33 g纯NaHCO3。
| 25℃ | NaHCO3 | Na2CO3 | NaOH |
| 溶解度/g | 9 | 33 | 110 |
(1)若用100 g水,则制取时需用NaOH g。
(2)若用17.86 g NaOH(固),则需用水 g。