不论以何种比例混合,将甲和乙两种混合气体同时通入过量的丙溶液中,一定能产生沉淀的组( )
| 序号 | ① | ② | ③ | ④ | ⑤ |
| 甲 | CO2 | HCl | CO2 | NO2 | CO2 |
| 乙 | SO2 | CO2 | SO2 | SO2 | NH3 |
| 丙 | 石灰水 | 石灰水 | Ba(NO3)2 | BaCl2 | CaCl2 |
|
| A. | ①②③④⑤ | B. | ②③④⑤ | C. | ①③④ | D. | ①②③④ |
下列反应所得的溶液中一定只含一种溶质的是( )
|
| A. | 向硫酸酸化的Fe2(SO4)3溶液中加入过量的Ba(OH)2溶液 |
|
| B. | 向AlCl3溶液中加入过量的氨水 |
|
| C. | 向NaOH溶液中通人CO2气体 |
|
| D. | 将过量的Cu粉加入FeCl3溶液 |
某无色透明酸性溶液,可能含有K+、Mg2+、Al3+、Cu2+、NH4+、Cl﹣、SO42﹣、NO3﹣中的几种,取该溶液三等份分别进行实验①加入少量Zn产生H2,②逐滴加人NaOH溶液,其加入量和沉淀生成量关系如图所示,③加入0.1mol/LBaCl2溶液至5ml时不再产生白色沉淀,取上层清液加入足量AgNO3溶液,得到0.287g沉淀,由此推知原溶液中( )
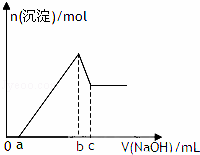
|
| A. | 一定没有Cu2+、NO3﹣、Cl﹣ | B. | 可能有K+、NH4+、NO3﹣、SO42﹣ |
|
| C. | 不能确定是否含有K+、NO3﹣ | D. | 一定有Mg2+、Al3+、Cl﹣、SO42﹣ |
已知同温同压下,下列反应的焓变和平衡常数分别表示为
H2(g)+ O2(g)=H2O(g)△H1 K1
O2(g)=H2O(g)△H1 K1
 N2(g)+O2(g)=NO2(g)△H2 K2
N2(g)+O2(g)=NO2(g)△H2 K2
 N2(g)+
N2(g)+ H2(g)=NH3(g)△H3 K3
H2(g)=NH3(g)△H3 K3
则反应2NH3(g)+ O2(g)=2NO2(g)+3H2O(g)的△H和K分别为( )
O2(g)=2NO2(g)+3H2O(g)的△H和K分别为( )
|
| A. | 2△H1+2△H2﹣2△H3 3K1+2K2﹣2K3 |
|
| B. | 2△H3﹣3△H1﹣2△H2 |
|
| C. | 3△H1+2△H2﹣2△H3 |
|
| D. | 3△H1+2△H2﹣2△H3 3K1+2K2﹣2K3 |
锑(Sb)在自然界中一般以硫化物的形式存在,我国锑的蕴藏量占世界第一.从硫化物中提取单质锑一般先在高温下将硫化物转化为氧化物,再用碳还原:关于反应①、②的说法正确的是( )
①2Sb2S3+3O2+6Fe Sb4O6+6FeS,
Sb4O6+6FeS,
②Sb4O6+6C 4Sb+6CO↑.
4Sb+6CO↑.
|
| A. | 反应①、②中的氧化剂分别是Sb2S3、Sb4O6 |
|
| B. | 反应①中每生成3molFeS时,共转移6 mol电子 |
|
| C. | 反应②说明高温下Sb的还原性比C强 |
|
| D. | 每生成4 molSb时,反应①与反应②中还原剂的物质的量之比为2:1 |
下列说法中正确的是( )
|
| A. | 难溶电解质的Ksp越小,溶解度就一定越小 |
|
| B. | 一般认为沉淀离子浓度小于1.0×10﹣5 mol/L时,沉淀就达完全 |
|
| C. | 用饱和Na2CO3溶液可以将BaSO4转化为BaCO3,说明Ksp(BaCO3)小于Ksp(BaSO4) |
|
| D. | 向含AgCl沉淀的悬浊液中加入NaCl饱和溶液,AgCl的溶解度变小,溶度积常数变小 |
下列解释事实的化学方程式或离子方程式不正确的是( )
|
| A. | 向饱和Na2CO3中加入过量CO2气体:CO32﹣+CO2+H2O=2HCO3﹣ |
|
| B. | 在沸水中滴入饱和FeCl3溶液制取Fe(OH)3胶体:Fe3++3H2O=Fe(OH)3(胶体)+3H+ |
|
| C. | 4mol/L的NaAlO2溶液和7mol/L的盐酸等体积混合:4AlO2﹣+7H++H2O=3Al(OH)3↓+Al3+ |
|
| D. | 酸化的KMnO4溶液与H2O2反应:2MnO4﹣+6H++5H2O2=2Mn2++5O2↑+8H2O |
下列离子在给定的条件下能大量共存的是( )
|
| A. | 饱和氯水中:Cl﹣、NO3﹣、Na+、SO32﹣ |
|
| B. | 常温下, |
|
| C. | 0.1 mol/L的NaOH溶液中:K+、AlO2﹣、SO42﹣、CO32﹣ |
|
| D. | 在PH=7的溶液中:Fe3+、Na+、Br﹣、Cl﹣ |

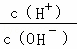 =1×1012的溶液中:Ca2+、Na+、I﹣、NO3﹣
=1×1012的溶液中:Ca2+、Na+、I﹣、NO3﹣