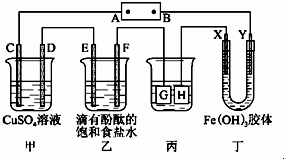
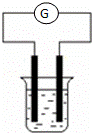
现有A、B、C、D和Cu五种金属片,将其分别用导线连接后浸入稀硫酸中(如图),每次实验时,通过灵敏电流计测出电子流动方向如下:
| G 实验分组 | 所用金属 | 电子流向 |
| ① | A、Cu | A→Cu |
| ② | C、D | D→C |
| ③ | A、C | C→A |
| ④ | B、Cu | Cu→B |
| ⑤ | … | … |
根据上述情况,回答下列问题:
(1)上述五种金属的活动性顺序是 .
(2)在①中,Cu片上观察到的现象是: ;
(3)在②中,溶液中H+向金属片 移动;
(4)在④中,两金属片上均无气泡放出.此时两金属片上的电极反应式分别为:Cu: ;B: ;
(5)如果实验⑤用B、D,则导线中电流方向为: (填B→D或D→B);
(6)已知反应:Cu+2Fe3+═Cu2++2Fe2+.请用下列试剂和材料,用上图所示装置,将此反应设计成原电池并检验正极产物.
试剂:CuCl2溶液、FeCl3溶液、FeCl2溶液、KSCN溶液、K3[Fe(CN)6]溶液、双氧水、NaOH溶液
材料:Cu片、Fe片、石墨棒
a、设计电池应选用的试剂和材料是: ;
b、检验正极产物选用的试剂是 ,检验反应的离子方程式: .
 ]>[NH
]>[NH ]
]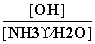 增大
增大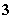 ===CaCO3↓+H2O
===CaCO3↓+H2O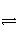
 H++CH3COO-,下列叙述不正确的是( )
H++CH3COO-,下列叙述不正确的是( )