0 14126 14134 14140 14144 14150 14152 14156 14162 14164 14170 14176 14180 14182 14186 14192 14194 14200 14204 14206 14210 14212 14216 14218 14220 14221 14222 14224 14225 14226 14228 14230 14234 14236 14240 14242 14246 14252 14254 14260 14264 14266 14270 14276 14282 14284 14290 14294 14296 14302 14306 14312 14320 203614
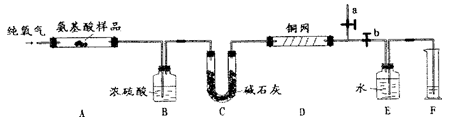





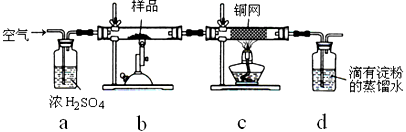
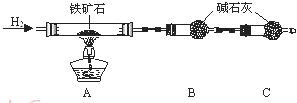

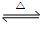 2SO2(g) + O2(g) 该反应的平衡常数表达式为K=____________。
2SO2(g) + O2(g) 该反应的平衡常数表达式为K=____________。